Das zweiteinfachste Alkan ist das Ethan C2H6, seine Konstitution kann beschrieben werden als "ein C-Atom, das über eine kovalente Einfachbindung mit einem zweiten C-Atom verbunden ist. Jedes der beiden C-Atome ist außerdem mit drei H-Atomen verbunden".
Strukturdaten
Alle Bindungswinkel im Ethan-Molekül betragen 109,5º. Dies entspricht genau dem Tetraederwinkel, der ja für das sp3-hybridisierte C-Atom charakteristisch ist . Die sechs C-H-Bindungen sind relativ unpolar, da der EN-Unterschied zwischen Kohlenstoff (2,55) und Wasserstoff (2,20) recht klein ist. Die C-C-Einfachbindung ist natürlich völlig unpolar!
Die Bindungslänge der C-H-Bindungen beträgt 109 pm, während die C-C-Bindung 154 pm lang ist. Das liegt daran, dass bei der C-C-Einfachbindung zwei lange sp3-Hybridorbitale überlappen, während bei der C-H-Bindung das sp3-Hybridorbital des C-Atoms mit dem kleinen s-Orbital des H-Atoms überlappt:
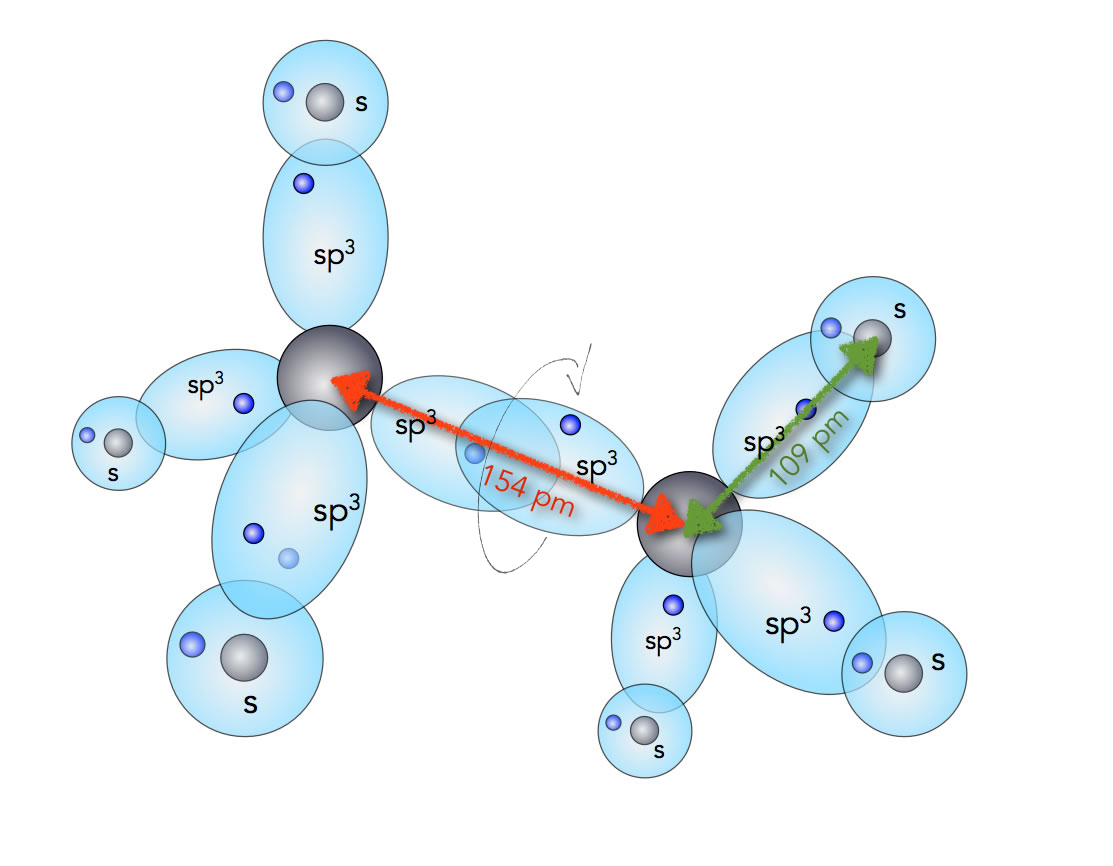
Die Bindungen im Ethan-Molekül
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Bei beiden Bindungsarten im Ethan-Molekül, also bei der C-C-Bindung wie auch bei der C-H-Bindung, handelt es sich um σ-Bindungen. Die Elektronendichte ist "symmetrisch um die Achse angeordnet, die die beiden bindenden Atome verknüpft" [1].
Aus diesem Grund ist es auch überhaupt kein Problem, wenn sich eine der beiden Methylgruppen des Ethan-Moleküls dreht, um die C-C-Bindung herrscht eine freie Drehbarkeit. Das gilt natürlich auch für die sechs C-H-Bindungen, was aber keine Rolle spielt, denn wenn sich ein H-Atom dreht, wirkt sich das in keiner Weise auf die Konformation des Moleküls aus. Was anderes ist es, wenn sich eine CH3-Gruppe dreht, dann ändert sich auch die Konformation (räumliche Anordnung) des Moleküls.
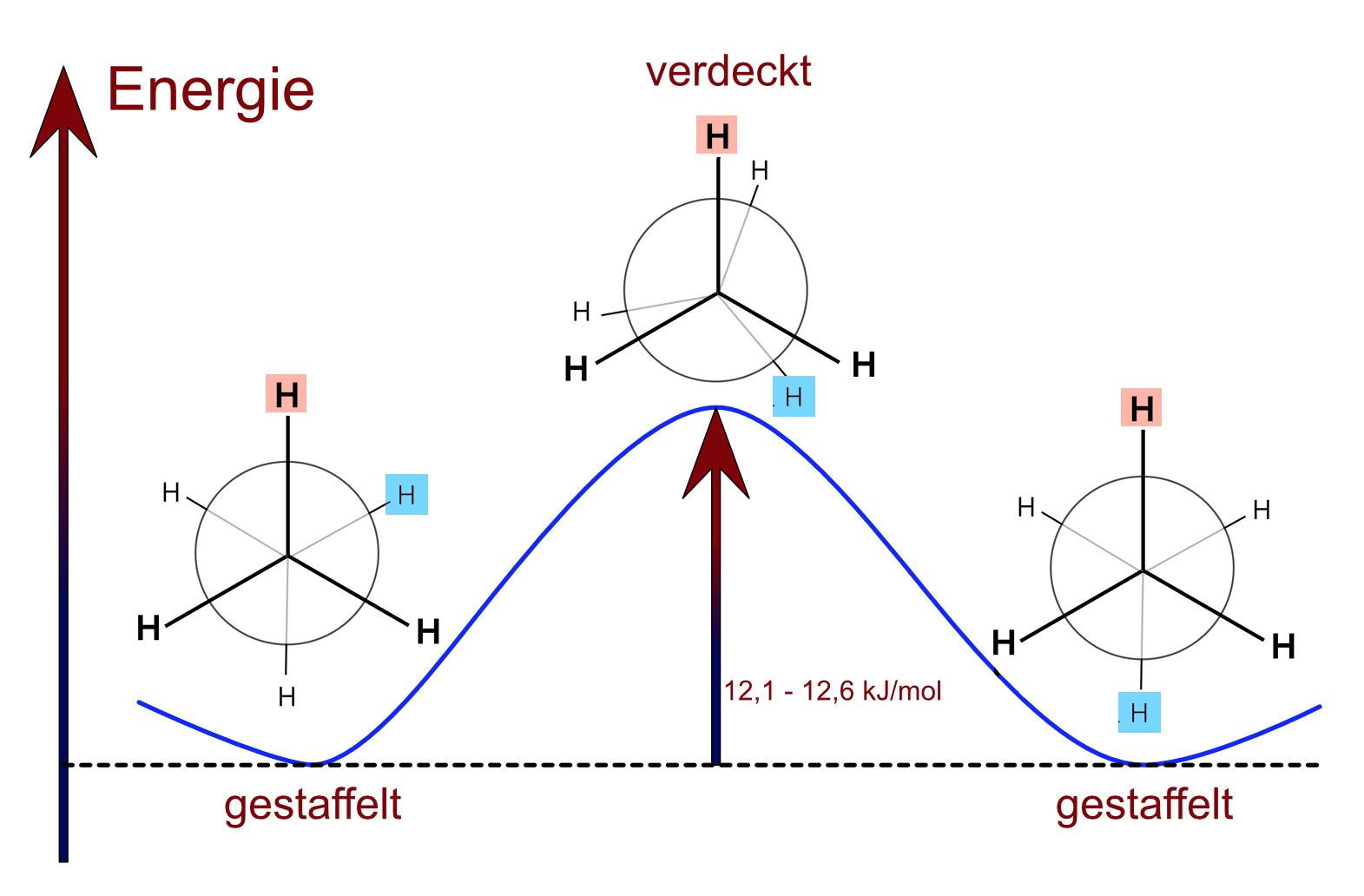
Die Ethan-Konformationen
Autor: Ulrich Helmich 2017, Lizenz: Public domain.
Die Torsionsenergie (Rotations- oder Drehungsenergie) des Ethans ist mit 12,1 bis 12,6 kJ/mol extrem klein. Die Folge davon ist, dass sich die beiden Methylgruppen des Moleküls bei Zimmertemperatur ständig um die C-C-Achse gegeneinander verdrehen. Allerdings gibt es ein Energieminimum, wenn das Ethan-Molekül in der sogenannten gestaffelten Konformation vorliegt. Diese Konformation ist besonders stabil, daher liegen ständig ca. 99% aller Ethan-Moleküle in dieser Konformation vor.
Quellen:
- M. A. Fox, J. K. Whitesell: Organische Chemie - Grundlagen, Mechanismen, bioorganische Anwendungen. 1. Auflage, Heidelberg 1995.
- K. P. C. Vollhard, N.E. Schore: Organische Chemie. 3. Auflage, Weinheim 2000.