Addition von HBr an Ethen
Zu diesem Thema gibt es jetzt eine Präsentation "Hydrobromierung", die Sie kostenlos hier herunterladen können.
Löst man Bromwasserstoff in Wasser, so findet eine Protolyse statt: Die HBr-Moleküle geben ein Proton an ein Wasser-Molekül ab, es bilden sich Oxonium-Ionen. Kommt ein solches Oxonium-Ion in die Nähe einer C=C-Doppelbindung, so wird ein Proton auf die Doppelbindung übertragen:
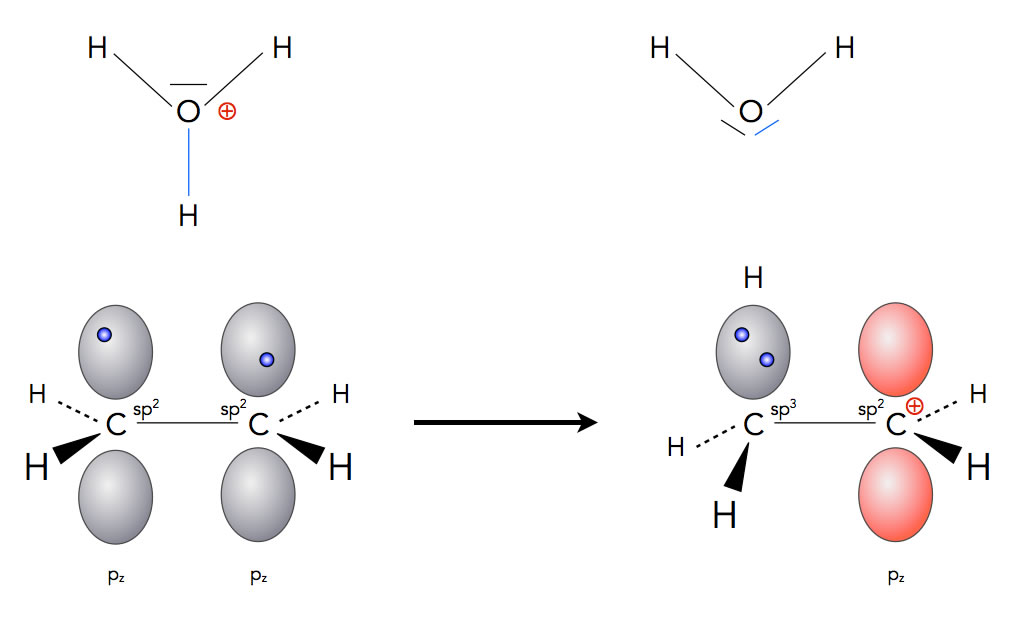
Der erste Schritt der Hydrobromierung in wässriger Lösung
Das Proton wird vom Oxonium-Ion abgespalten, bildet eine kovalente Bindung mit einem der beiden C-Atome der Doppelbindung aus, und das andere C-Atom wird zum Carbenium-Ion.
Konkurrenzreaktion mit Wasser
In einer wässrigen Lösung sind auch immer Hydroxid-Ionen anwesend. Wegen ihrer negativen Ladung werden Hydroxid-Ionen von einem Carbenium-Ion angezogen. Wenn das passiert, entsteht kein Brom-Alkan, sondern ein Alkohol.
Wenn Sie mehr über dieses Thema erfahren wollen, sollten Sie sich die Seite ansehen, die ich speziell für die Abteilung "Studienvorbereitung Organische Chemie" geschrieben habe.
Die Markownikow-Regel
Der russische Forscher Wladimir W. Markownikow entdeckte 1869, dass sich bei der Addition von Halogenwasserstoffen an Alkene das H-Atom immer an dasjenige C-Atom setzt, das bereits mit den meisten H-Atomen verbunden ist. Hier ein klassisches Beispiel:
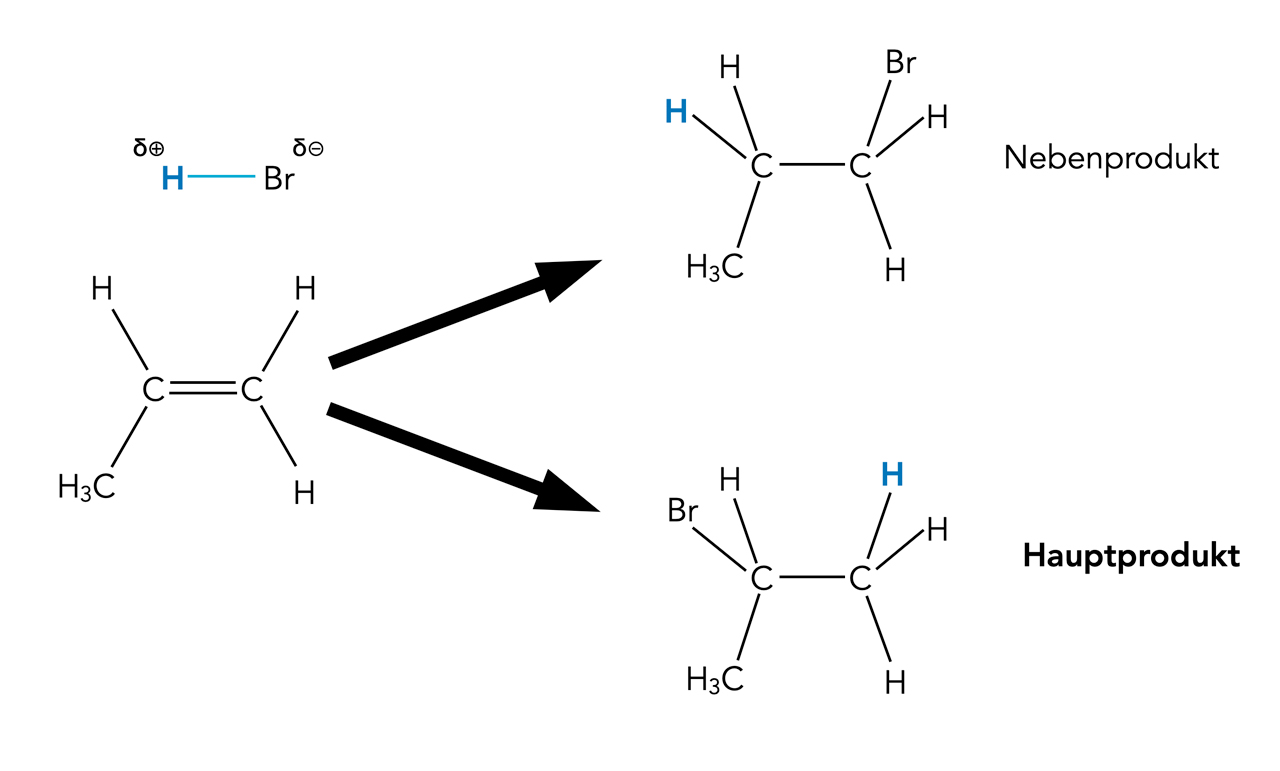
Addition von Bromwasserstoff an Propen
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Das rechte C-Atom des Propen-Moleküls in der Abbildung besitzt zwei H-Atome, das linke C-Atom nur eins. Der Wasserstoff des HBr-Moleküls setzt sich daher an das rechte C-Atom und nur im Ausnahmefall an das linke.
Heute weiß man, dass diese frühe Markownikow-Regel auf die unterschiedliche Stabilität von Carbenium-Ionen zurückzuführen ist. Das Proton des Halogenwasserstoff-Moleküls setzt sich so an die C=C-Doppelbindung, dass immer das jeweils stabilste Carbenium-Ion entsteht:
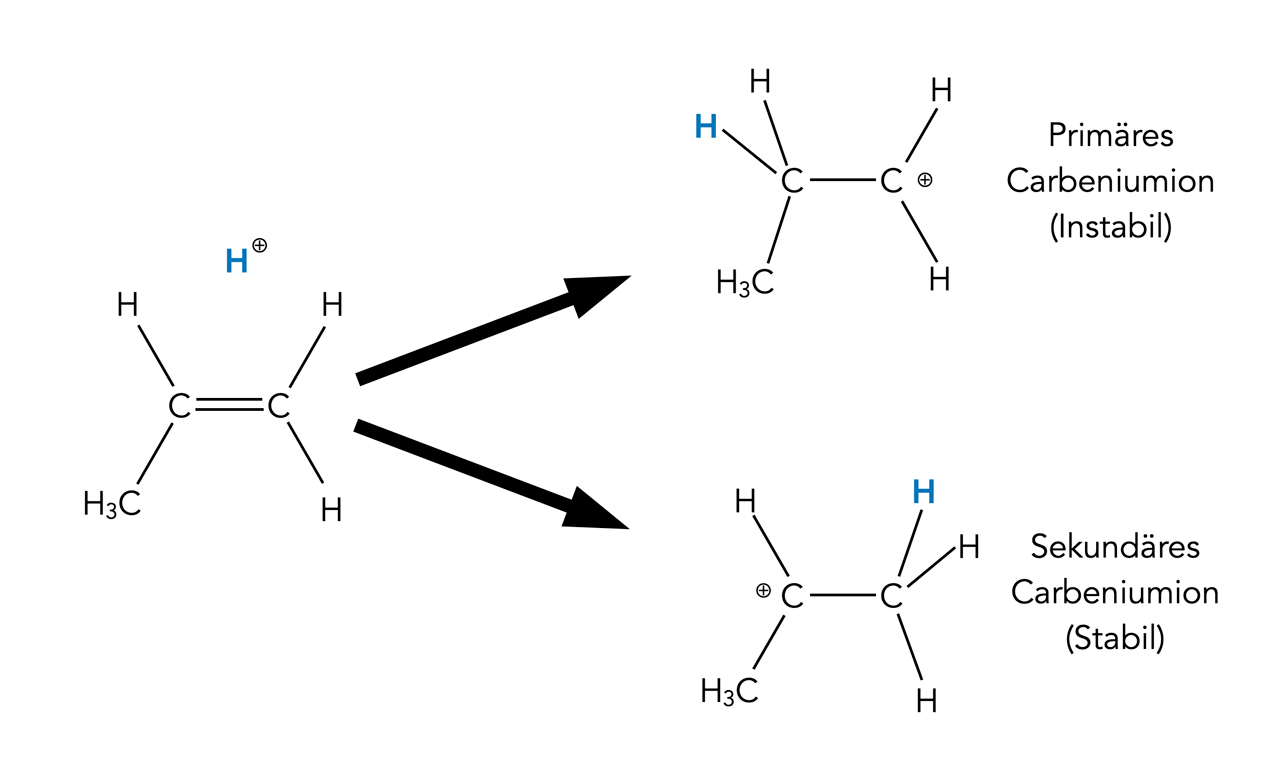
Sekundäre Carbenium-Ionen sind stabiler als primäre
Autor: Ulrich Helmich 2022, Lizenz: Public domain
Auf dieser Lexikon-Seite finden Sie weitere Einzelheiten zur Markownikow-Regel und auch Hinweise zur Schreibweise des Namens.
Quellen und weiterführende Bücher und Artikel, die über allgemeines Schulbuchwissen hinausgehen:
- M. A. Fox, J. K. Whitesell: Organische Chemie - Grundlagen, Mechanismen, bioorganische Anwendungen. 1. Auflage, Heidelberg 1995.
- K. P. C. Vollhard, N.E. Schore: Organische Chemie. 6. Auflage, Weinheim 2020.
- J. Clayden, N. Greeves, S. Warren: Organische Chemie. Berlin 2013.
- R. T. Morrison, R. N. Boyd, S. K. Bhattacharjee: Organic Chemistry. 7. Auflage, Dorling Kindersley 2011.
- Reinhard Brückner, Reaktionsmechanismen, 3. Auflage, Springer-Verlag 2014.
- Organikum, 22. Auflage, Weinheim 2004.
- J. Falbe, M. Regitz (Herausgeber): Römpp Chemie Lexikon in 6 Bänden. 9. Auflage, Stuttgart, New York 1989-1992.