KI-Zusammenfassung
Die Zink-Kohle-Batterie ist eine einfache galvanische Zelle, in der chemische Energie in elektrische Energie umgewandelt wird. Am Minuspol wird Zink oxidiert und gibt Elektronen ab; diese fließen durch den äußeren Stromkreis zum Pluspol. Dort wird Mangan(IV)-oxid reduziert, während im Elektrolyten weitere Reaktionen mit Ammonium-Ionen und Chlorid-Ionen ablaufen. Der Graphitstab dient dabei nicht als eigentlicher Reaktionspartner, sondern als Leiter für die Elektronen. Insgesamt beruht die Funktion der Batterie also auf gekoppelten Redoxreaktionen an den Elektroden und zusätzlichen Reaktionen im Elektrolyten.
Aufbau
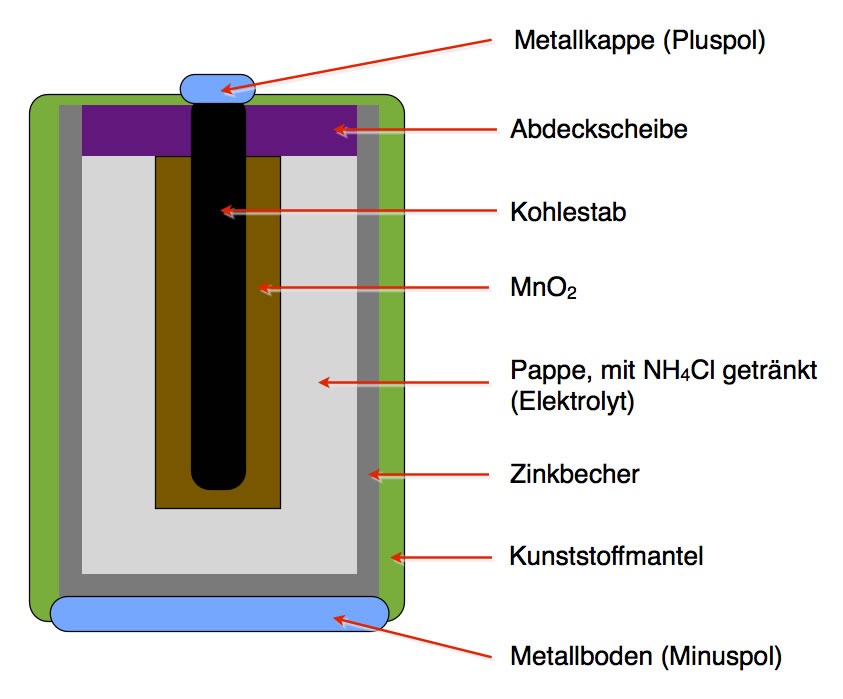
Hier sehen wir eine vereinfachte Schemazeichnung einer Zink-Kohle-Batterie im Längsschnitt. Das sogenannte Leclanché-Element wurde um 1865 von Georges Leclanché (1839-1882) entwickelt. Eigentlich sollte es jedoch eher als Zink-Braunstein-Element bezeichnet werden, denn nicht der Kohlenstoff nimmt an den chemischen Reaktionen teil, sondern der Braunstein MnO2. Der Graphit-Stab in der Mitte der Batterie dient nur dazu, die Elektronen zum Braunstein zu leiten.
Reaktionen
Reaktionen an der Anode
Die Reaktionen am Minuspol, der Anode, sind zunächst recht einfach. Das Zink wird oxidiert und gibt dabei je Atom zwei Elektronen ab:
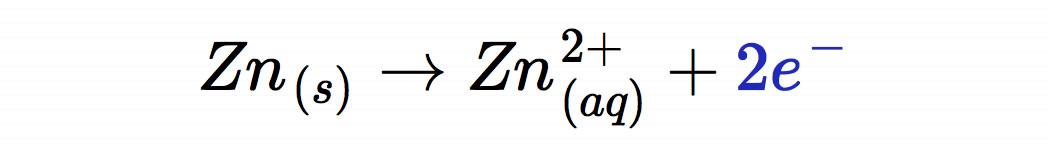
Mit den Begriffen "Anode" und "Kathode" muss man vorsichtig sein. Bei einer Elektrolyse ist die Anode der Pluspol. Dort findet die Oxidation statt. Die Kathode ist dann der Minuspol; dort findet die Reduktion statt.
Bei einer Batterie oder allgemeiner bei einem galvanischen Element ist es umgekehrt. Auch hier ist die Anode die Elektrode, an der die Oxidation stattfindet, sie ist jetzt aber der Minuspol. Die Kathode ist entsprechend der Pluspol. Bei galvanischen Elementen und Batterien ist die Anode also der Minuspol, die Kathode der Pluspol.
Reaktionen an der Kathode
Was passiert nun am Pluspol der Batterie, der Kathode? Hier wird das Mangan(IV)-oxid zu Mangan(III)-oxid-hydroxid reduziert:
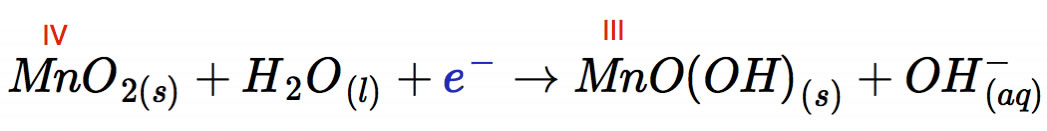
Da bei der Oxidation eines Zink-Atoms zwei Elektronen abgegeben werden, muss diese Reaktion für jedes oxidierte Zink-Atom zweimal ablaufen.
Die Zahlen IV und III über den Symbolen in der obigen Reaktionsgleichung geben die Oxidationszahlen an. Wenn Sie nicht mehr wissen, wie man die Oxidationszahl eines Atoms oder Ions bestimmt, sollten Sie auf diese Seite gehen und sich dort informieren.
Reaktionen im Elektrolyten
Neben diesen beiden Primärreaktionen laufen im Elektrolyten der Zink-Braunstein-Batterie weitere Reaktionen ab, die für die Funktion der Batterie wichtig sind.
Die technische Umsetzung der verschiedenen Typen dieser Batterie ist oft unterschiedlich, aber allen gemeinsam ist ein Elektrolyt, der Ammoniumchlorid enthält. Ob es sich nun wie in der obigen Zeichnung um eine mit Ammoniumchlorid-Lösung getränkte Pappe oder um eine Ammoniumchlorid-haltige Paste handelt, ist im Prinzip zweitrangig.
Die bei der Reduktion gebildeten Hydroxid-Ionen reagieren mit den Ammonium-Ionen des Elektrolyten:
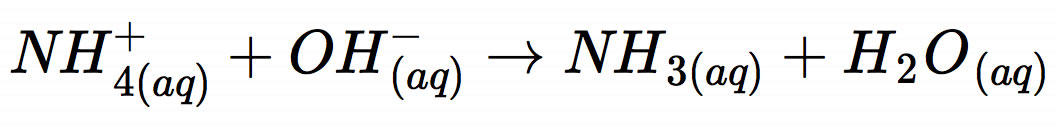
Bei dieser klassischen Protolyse entsteht Ammoniak, ein stechend riechendes und giftiges Gas, das hier zunächst noch im Elektrolyten gelöst ist. Aber keine Sorge: Die Ammoniak-Moleküle reagieren dann mit den Zink-Ionen und werden dadurch chemisch gebunden:
![Zn2+ + 2 NH3 ==> [Zn(NH3)2]2+](Bilder/ZnC05.jpg)
Diese Reaktion ist weder eine Protolyse noch eine Redoxreaktion, sondern eine Komplexbildungsreaktion. Zwei oder mehrere Moleküle oder Ionen lagern sich zu einem komplexeren Teilchen zusammen, ohne dass dabei Protonen oder Elektronen von einem Donator zu einem Akzeptor übertragen werden. Mit dem Kugelwolkenmodell kann man solche Reaktionen leider nicht erklären, da hier Atomorbitale eine Rolle spielen, die im Kugelwolkenmodell nicht berücksichtigt werden.
Die gelösten Komplex-Kationen verbinden sich nun mit den Chlorid-Ionen der Elektrolyt-Lösung zu einem schwerlöslichen Feststoff:
![[Zn(NH3)2]2+ + 2 Cl- ==> [Zn(NH3)2]Cl2](Bilder/ZnC06.jpg)
Das Ganze schauen wir uns nun noch einmal in einem zusammenfassenden Schema an:
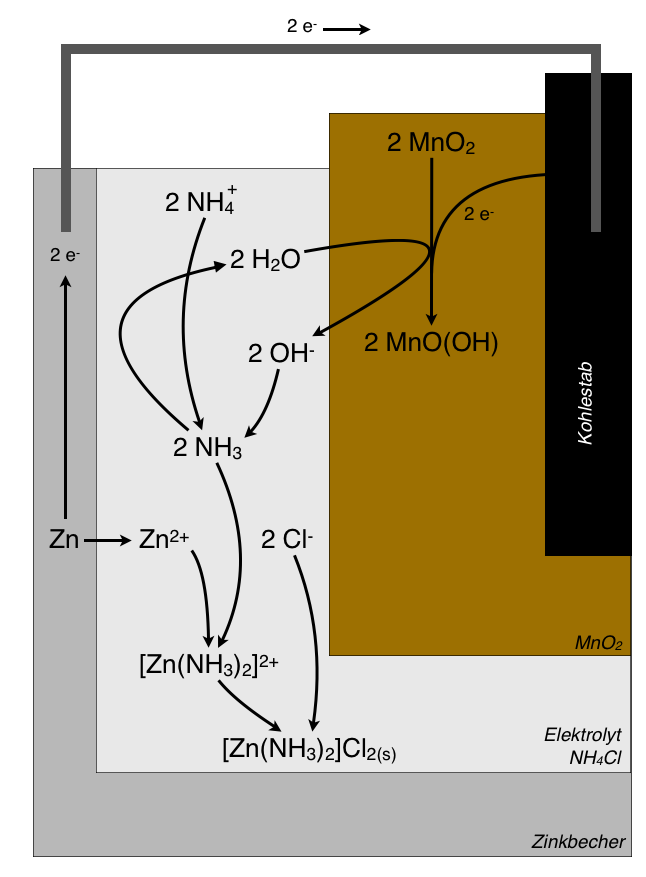
Dieses Schema fasst die zuvor erläuterten Teilreaktionen noch einmal zusammen.