Kondensation
Als Kondensation bezeichnet man allgemein eine chemische Reaktion, bei der sich zwei Moleküle unter Abspaltung eines kleineren Produktes zu einem größeren Endprodukt vereinigen.
Meistens handelt es sich bei dem abgespaltenen Produkt um Wasser. Ein einfaches Beispiel für eine solche Kondensation aus der Biochemie ist die Kondensation von zwei Aminosäuren zu einem Dipeptid:
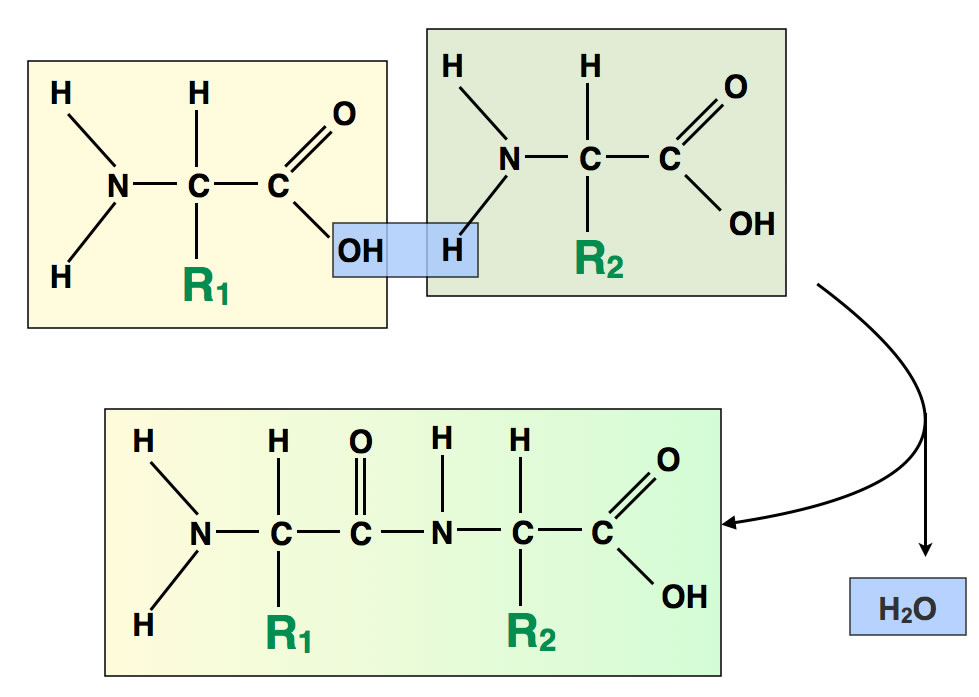
Weitere Einzelheiten zum Thema "Aminosäuen, Peptide und Proteine" finden Sie auf den Zellbiologie-Seiten dieser Homepage. In der Biochemie bzw. Zellbiologie kommen überhaupt recht viele Kondensationsreaktionen und auch Polykondensationen vor, wenn sich zum Beispiel Tausende von Glucose-Molekülen zu einem Stärke-Molekül zusammenschließen oder Zehntausende von Nucleodiden zu einem DNA-Strang.
Polykondensation
Damit eine Polykondensation stattfinden kann, also der Zusammentritt vieler Moleküle unter Abspaltung von Wasser oder anderen kleinmolekularen Produkten, müssen die Monomere zwei funktionelle Gruppen haben, die in der Lage sind, Atome oder Atomgruppen abzugeben. Geradezu prädestiniert dafür sind OH-Gruppen und COOH-Gruppen sowie NH2-Gruppen.
Polyester
Polyester sind Kunststoffe, die aus dem Alltag nicht mehr wegzudenken sind. Nicht nur Textilfasern wie Trevira, Diolen und so weiter sind Polyester, sondern auch PET-Getränkeflaschen (Aufmacherbild), CDs, DVDs und BlueRays werden aus Polyestern hergestellt.
Es gibt grundsätzlich zwei Möglichkeiten, einen Polyester herzustellen. Ein Ester ist ja eine Verbindung aus einer Sauerstoffsäure und einem Alkohol. Ein Polyester besteht aus vielen Säure- und Alkohol-Molekülen, die abwechselnd miteinander verbunden sind. Jedes Alkohol-Molekül ist mit zwei Säure-Molekülen verbunden, muss daher also zwei OH-Gruppen besitzen. Jedes Säure-Molekül ist mit zwei Alkohol-Molekülen verbunden, und muss folglich zwei COOH-Gruppen besitzen. Wir können also einen ganz einfachen Polyester herstellen (zumindest in der Theorie), wenn wir einen zweiwertigen Alkohol (z.B. Ethan-1,2-diol) mit einer Dicarbonsäure (z.B. Oxalsäure) koppeln.
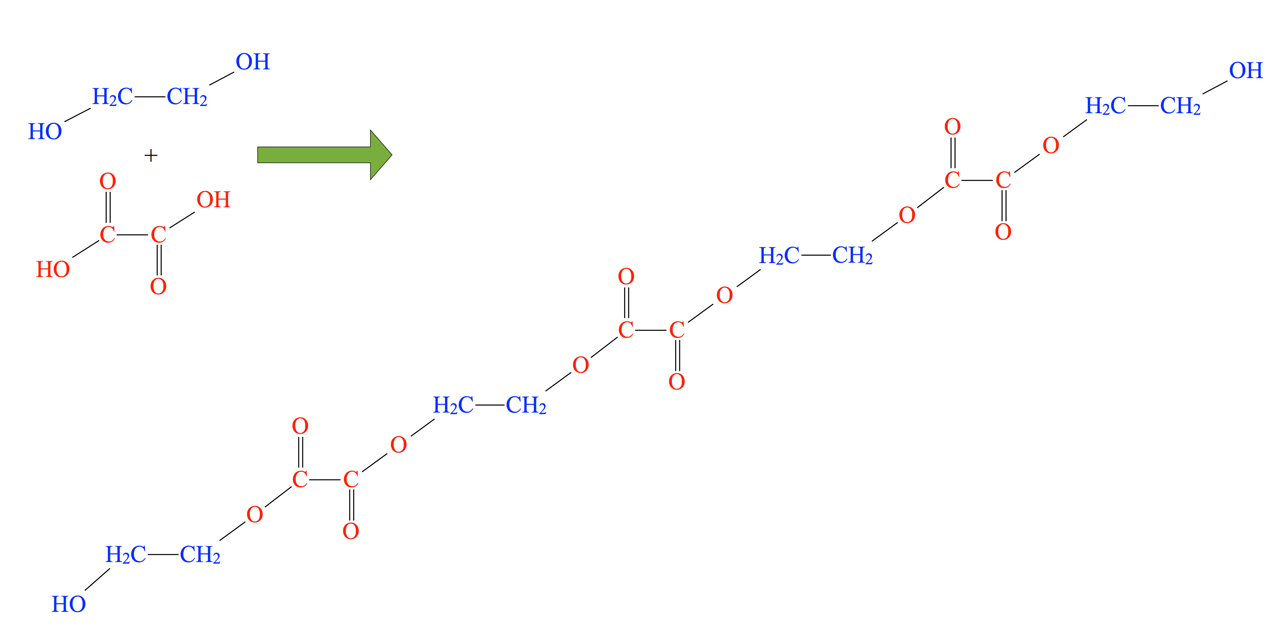
Das obere Bild zeigt einen "Minipolyester" aus vier Molekülen Glycol (Ethan-1,2-diol) und drei Molekülen Oxalsäure. Die untere Abbildung zeigt das verallgemeinerte Grundprinzip der Polyesterbildung.
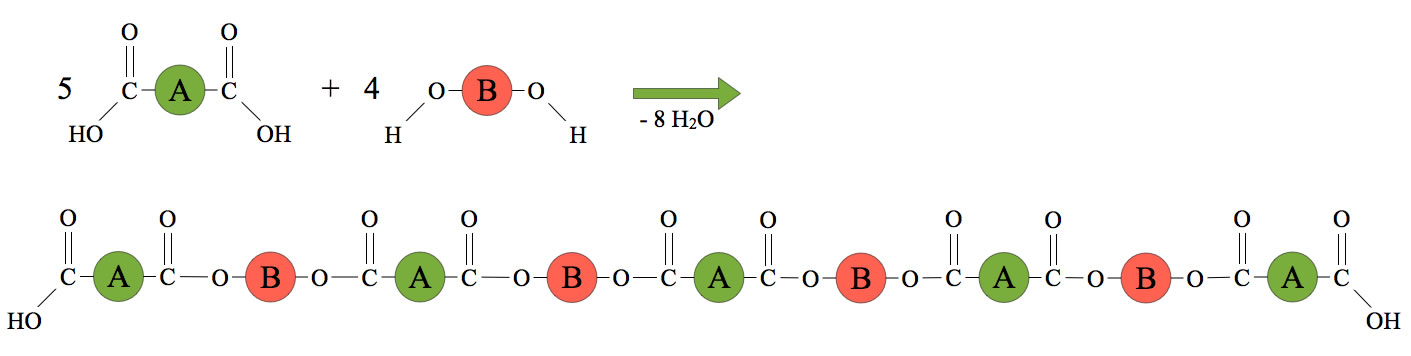
In der Abbildung haben nur 5 Säure- und 4 Alkohol-Moleküle reagiert, bei einem "echten" Polyester kondensieren Tausende solcher Monomere.
Besitzt die Carbonsäure drei Carboxylgruppen (wie zum Beispiel Zitronensäure) oder der Alkohol drei OH-Gruppen (wie zum Beispiel Glycerin), so können sich sogar verzweigte Polyester bilden, die dann natürlich viel stabiler sind als unverzweigte Polyester.
Einer der bekanntesten Polyester ist PET, die Abkürzung für Polyethylenterephthalat. Diese Verbindung ist ein Polymer aus Ethan-1,2-diol (Ethylenglycol) und der Terephthalsäure, einem Benzolring mit zwei Carboxylgruppen.
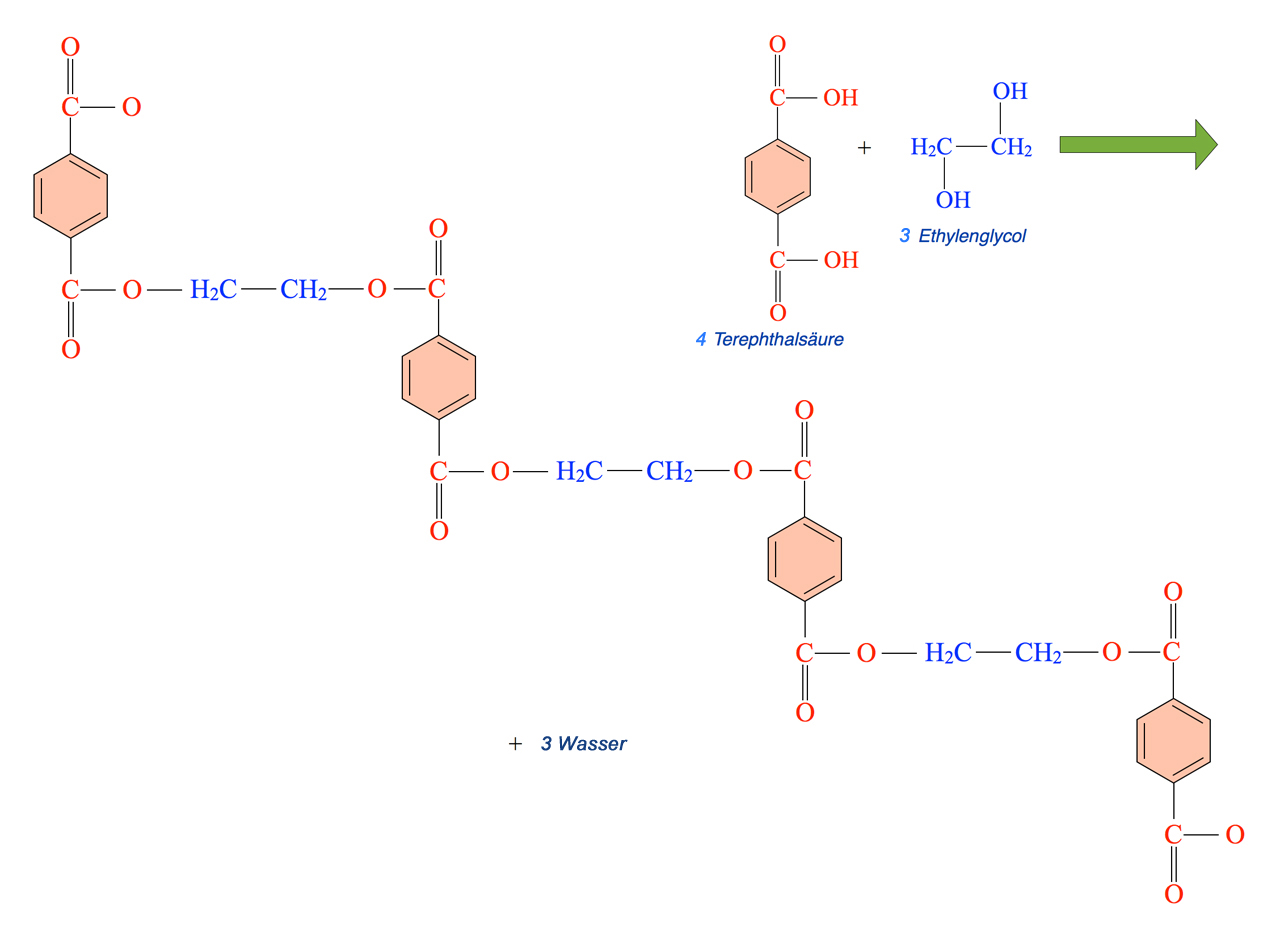
Hier sieht man ein "Mini-PET-Molekül", bestehend aus vier Molekülen der Dicarbonsäure und drei Molekülen des Diols. PET ist ein thermoplastischer Kunststoff, der vor allem durch die PET-Flaschen berühmt geworden ist, in denen heute fast alle Getränke verkauft werden.
Aus dem PET-Kunststoff kann man aber auch dünne Fasern ziehen (Thermoplast!), die dann unter dem Handelsnamen Trevira oder Diolen als Textilfasern bekannt sind.
Bakelit
Der Kunststoff Bakelit war das erste Polymer, das durch Polykondensation hergestellt wurde und gleichzeitig einer der ältesten Kunststoffe überhaupt, denn Bakelit wurde bereits 1872 synthetisiert. Nähere Einzelheiten…
Polyamide
Polyamide entstehen, wenn eine Dicarbonsäure mit einem Diamin, einem zweifachen Amin verestert wird.
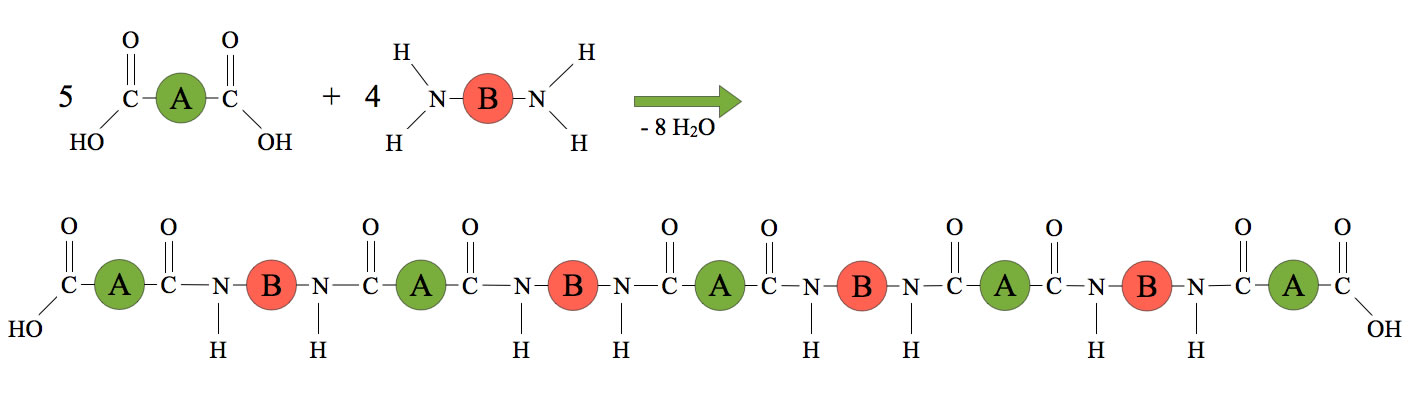
Hier sehen wir das Grundprinzip dieser Polymerisation am Beispiel eines "Mini-Polyamids" aus fünf Diol-Molekülen und vier Diamid-Molekülen.
Bekannte Polyamid-Kunststoffe sind die Textilfasern Perlon und Nylon, aus denen nicht nur Bekleidung hergestellt wird, sondern auch dicke Seile und Taue sowie Bodenbeläge. Bei der Bildung des Polyamids entstehen übrigens Peptidbindungen, die mit denen der Proteine identisch sind.
Nylon
Die Kunstfaser Nylon (1934 zum ersten Mal hergestellt) entsteht durch Polykondensation der Dicarbonsäure Adipinsäure (1,6-Hexandisäure) und des Diamids Hexamethylendiamin (1,6-Diaminohexan), also recht großen Monomeren mit je sechs C-Atomen.
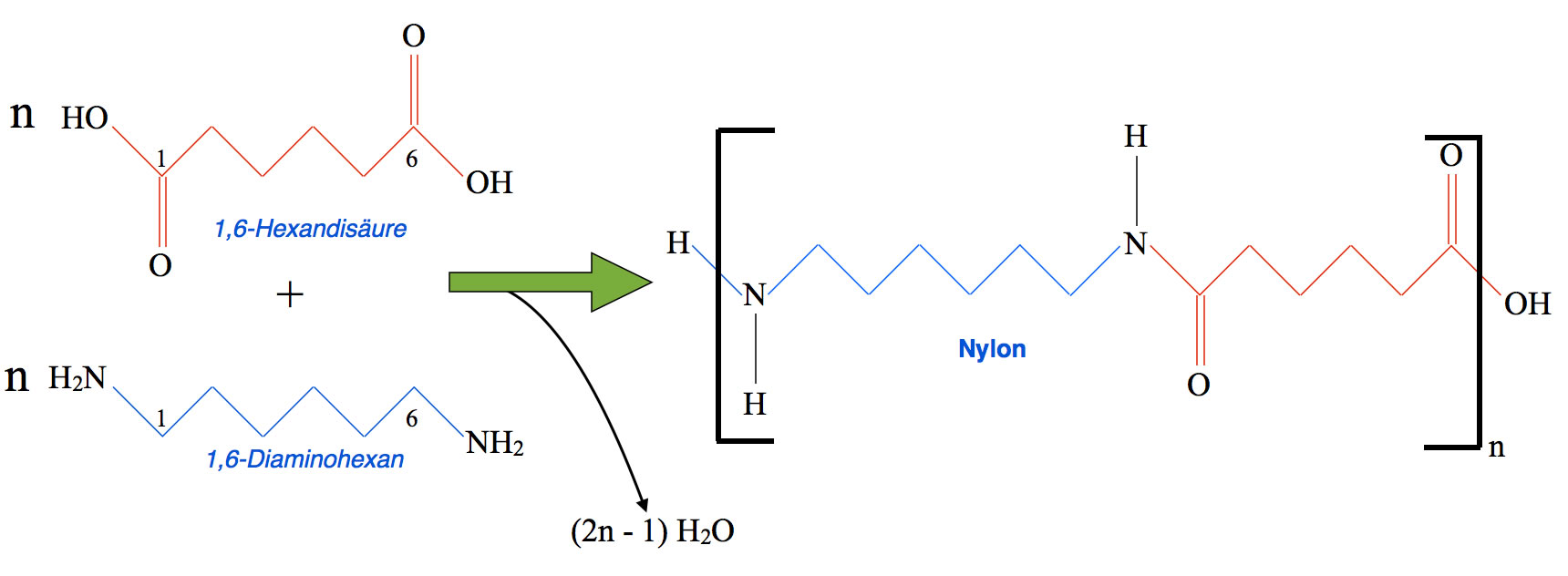
Hier sieht man die Bildung von Nylon aus 1,6-Hexandisäure und 1,6-Diaminohexan. Nylon ist ein Thermoplast. Der Kunststoff wird im flüssigen Zustand durch feine Düsen gepresst und härtet dann zu Kunstfasern aus. Dabei wird der Kunststoff mit flüssigem Stickstoff gekühlt. Die so erhaltenen Fasern werden dann vorsichtig (langsam) gedehnt, bis das handelsfertige Nylon entsteht. Bei diesem "Strecken" richten sich die Polymerketten mehr oder weniger parallel aus, zwischen den H-Atomen der ehemaligen Aminogruppen und den O-Atomen der ehemaligen Carboxylgruppen können sich H-Brücken bilden, so dass der gestreckte Nylonfaden deutlich stabiler ist als das Rohprodukt.
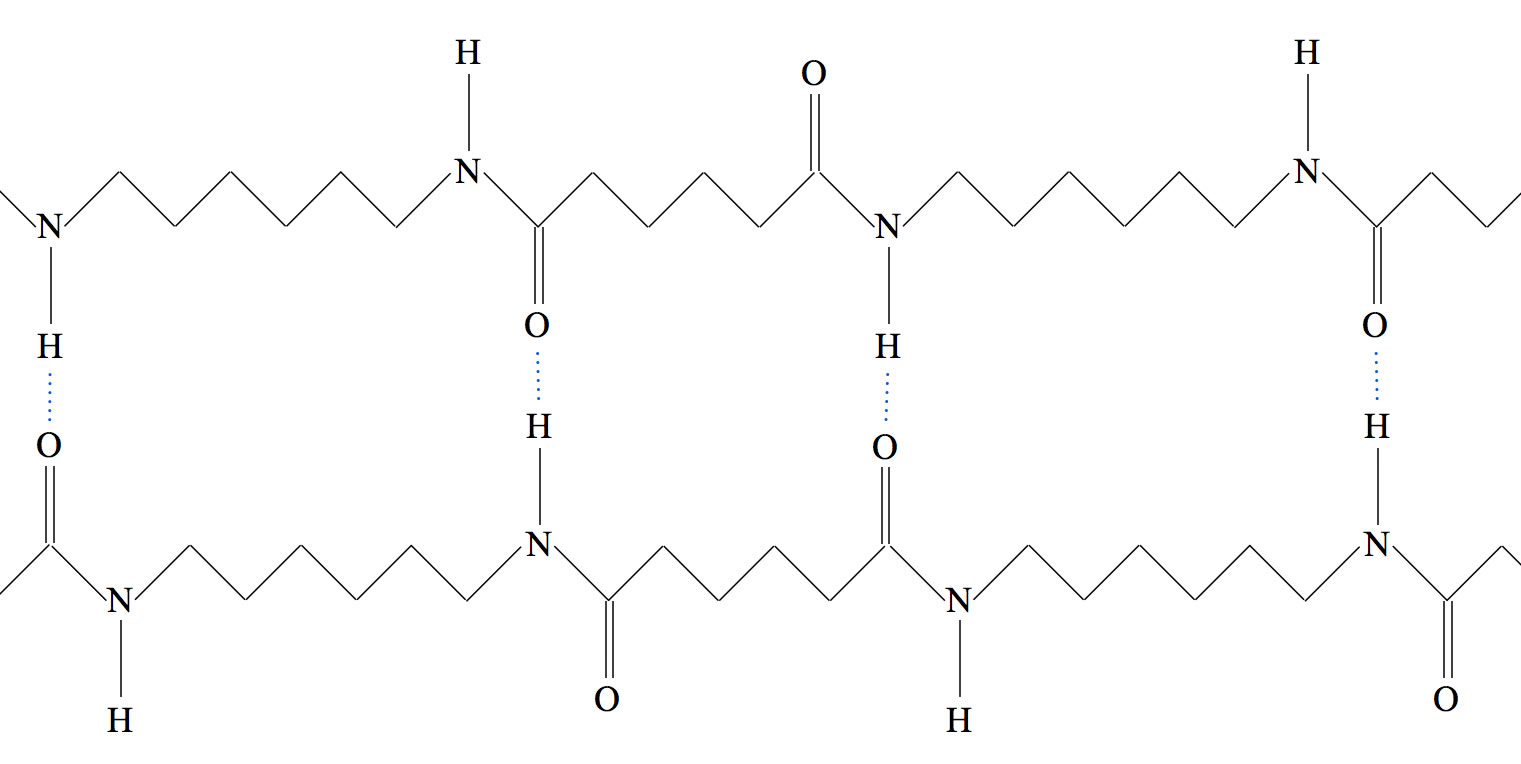
Hier sieht man die H-Brücken zwischen zwei dieser gestreckten Polymerfäden.
Polycarbonate
Polycarbonate gewinnt man aus Phosgen, einem Chlorderivat der Kohlensäure, bei dem beide OH-Gruppen durch Cl-Atome ersetzt sind, und einem Bisphenol, also einem Alkan-Derivat mit zwei Phenol-Gruppen. Der einfachste Bisphenol ist Bisphenol A, der aus Phenol und Aceton synthetisiert werden kann.
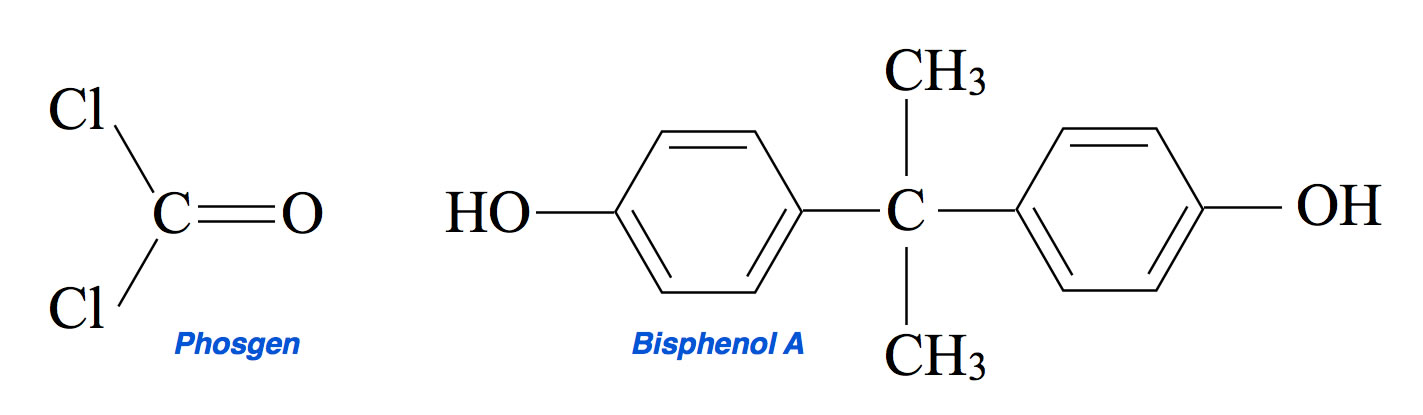
Das Polykondensationsprodukt der beiden Edukte wird als Polycarbonat bezeichnet, hauptsächlich deswegen, weil das Phosgen ein Kohlensäure-Derivat ist und weil die Salze der Kohlensäure Carbonate heißen. Bei der Kondensationsreaktion werden die beiden Chlor-Atome abgegeben, sie reagieren mit den H-Atomen der OH-Gruppen zu Chlorwasserstoff.
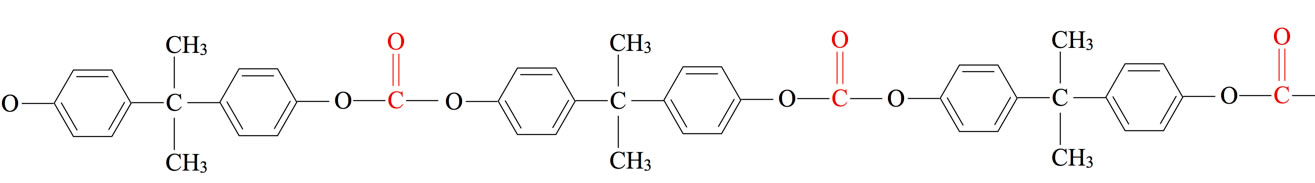
Hier sehen wir einen Ausschnitt aus einem solchen Polycarbonat-Polymer. Polycarbonate sind einerseits mechanisch sehr stabil, andererseits können sie sehr durchsichtig hergestellt werden. Daher eignen sie sich hervorragend für Brillen oder CDs und DVDs. Sogar Schutzhelme werden aus Polycarbonaten hergestellt.
Bisphenol A ist wahrscheinlich gesundheitsgefährend
Bisphenol A ist übrigens eine Substanz, die immer wieder in die Schlagzeilen der Presse kommt, weil doch recht viele gesundheitliche Gefahren von ihr ausgehen. Vor allem für die verringerte Fruchtbarkeit vieler Frauen und Männer soll die Freisetzung von Bisphenol A aus verschiedenen Kunststoffen verantwortlich sein. Es gibt Studien, die diese Vermutung bestätigen, andere Studien wiederum finden keinen Zusammenhang - typisch für Studien, die teils von Umweltschutzverbänden, teils von der Industrie finanziert werden. Zumindest hat im Jahre 2011 das Bundesministerium für Ernährung, Landwirtschaft und Verbraucherschutz Babyflaschen verboten, die Bisphenol A-Kunststoffe enthalten.
Seitenanfang -
Allgemeines -
Thermplaste -
Duroplaste -.
Elastomere -
Polymerisation -
Polyaddition - Polykondensation -
Beispiele -
Abitur
