Allgemeines
Unter dem Begriff Konformation versteht man räumliche Anordnung der Atome innerhalb eines Moleküls.
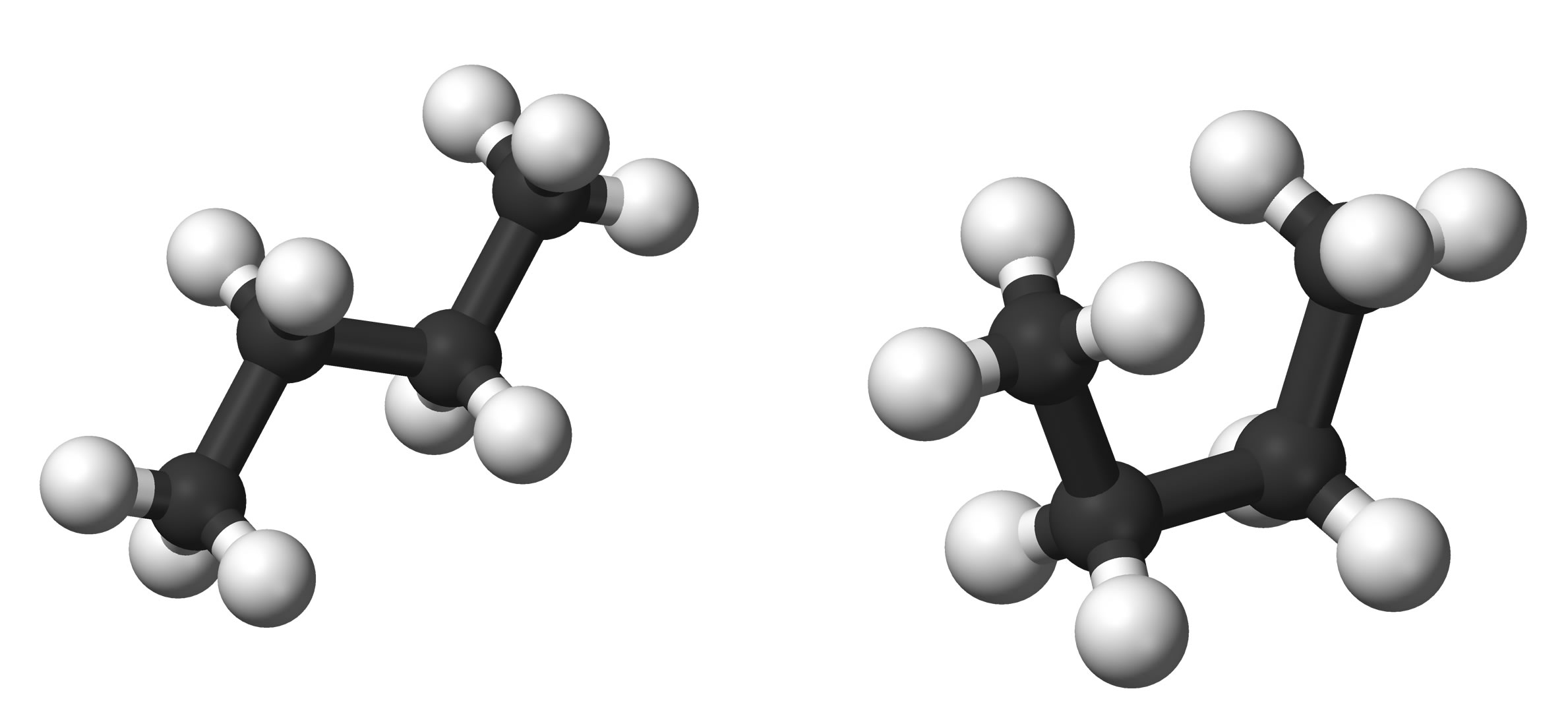
Zwei Konformationen des n-Butans
This work has been released into the public domain by its author, Benjah-bmm27.
Am Beispiel des n-Butans soll der Unterschied zwischen den Begriffen Konstitution und Konformation verdeutlicht werden.
Konstitution des n-Butans:
Vier C-Atome sind durch drei C-C-Einfachbindungen verbunden und bilden eine Kette. Die beiden äußeren C-Atome sind mit drei H-Atomen verknüpft, die beiden inneren C-Atome mit jeweils zwei H-Atomen.
Konformation des n-Butans links im Bild:
Die vier C-Atome bilden eine mehr oder weniger langgestreckte Kette.
Konformation des n-Butans rechts im Bild:
Die vier C-Atome bilden eine Art U; das 1. und das 4. C-Atom sind nach oben ausgerichtet, die C-Atome 2 und 3 liegen weiter unten.
Diese zwei Beschreibungen sind natürlich recht ungenau, aber an sich müssten Sie jetzt verstanden haben, was mit dem Begriff Konformation gemeint ist.
Stabilität von Konformeren
Schauen wir uns einmal verschiedene Konformationen des Ethan-Moleküls in einer besonderen Darstellungweise an, der sogenannten Newman-Projektion:
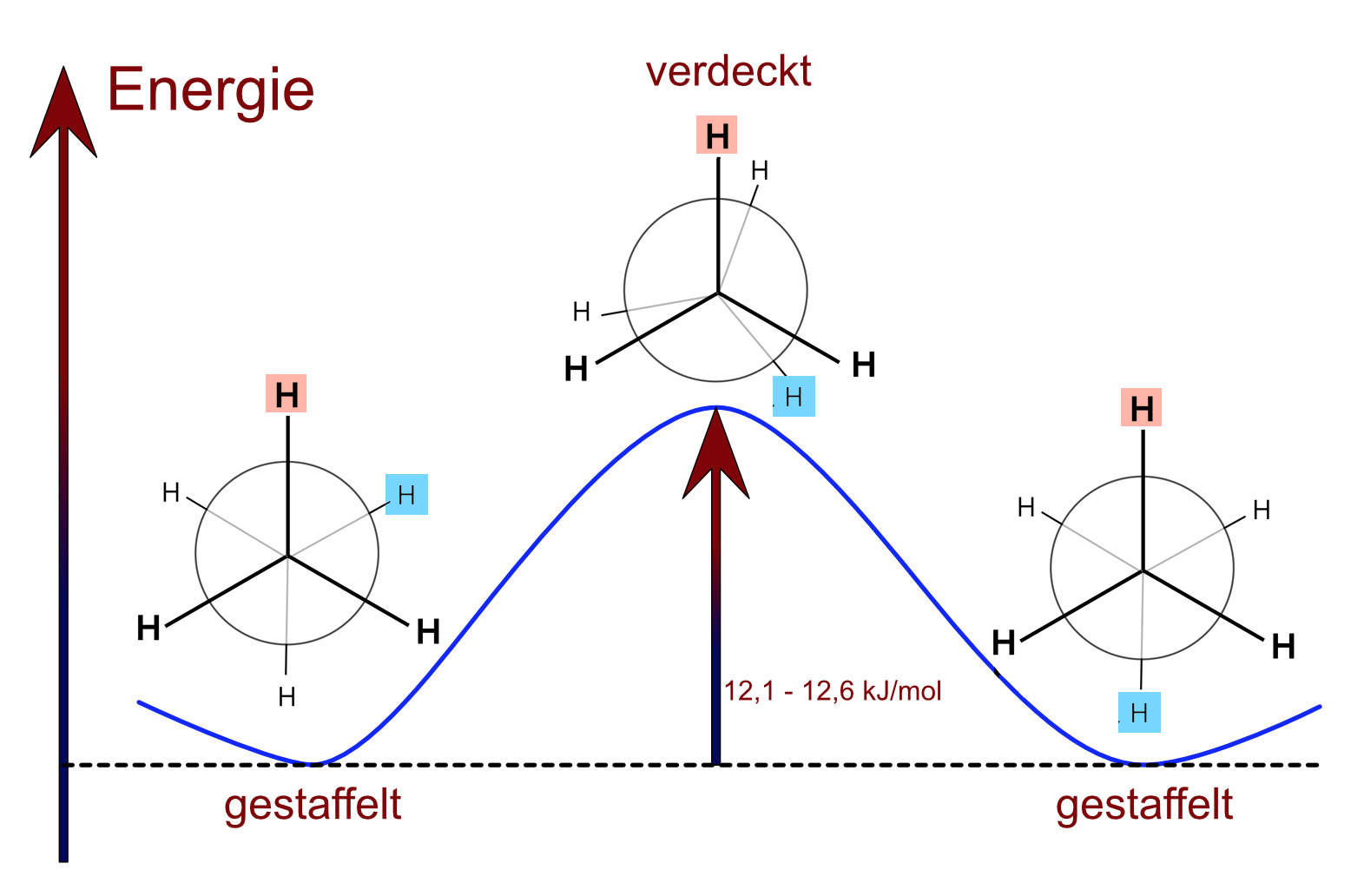
Konformationen des Ethan-Moleküls.
Dieses Werk ist lizenziert unter einer Creative Commons Namensnennung - Nicht-kommerziell - Weitergabe unter gleichen Bedingungen 4.0 International LizenzOffensichtlich haben die beiden gezeigten Konformationen, die gestaffelte und die verdeckte, eine unterschiedlich hohe innere Energie. Die gestaffelte Konformation ist energetisch günstiger als die verdeckte. Das liegt an der Abstoßung der Elektronenpaarbindungen zwischen den C- und den H-Atomen.
Bei komplexeren Molekülen gibt es viele verschiedene energetisch günstige Konformationen und noch mehr energetisch ungünstige Konformationen.
Konformation von Enzymen
In der Biologie ist der Begriff der Konformation vor allem bei der Enzymatik wichtig. Viele Enzyme können in zwei oder mehreren verschiedenen stabilen (= energetisch günstigen) Konformationen vorliegen. In der einen Konformation kann das Enzym gut arbeiten, in der anderen nicht so gut. Das liegt an dem Schlüssel-Schloss-Prinzip, das ja der Enzymwirkung zu Grunde liegt. In der stabilen Konformation A kann das Substrat des Enzyms passgenau aufgenommen werden (der Schlüssel passt), in der stabilen Konformation B passt das Substrat nicht in das aktive Zentrum des Enzyms. Kleine Effektor-Moleküle können dann beeinflussen, in welcher der beiden stabilen Konformationen das Enzym gerade vorliegt. Dies ist das Grundprinzip der allosterischen Enzymregulation.