Vorbemerkungen
Den passiven Transport durch Kanalproteine haben wir ja bereits im Zusammenhang mit der "normalen" Diffusion kennengelernt. Auf dieser Seite möchte ich noch einmal näher auf das Thema Kanalproteine, Ionenkanäle etc. eingehen. Wichtig ist, dass Kanal- bzw. Porenproteine nur den passiven Transport erlauben, also den Transport von Teilchen in Richtung eines Konzentrationsgefälles oder den "Bergabtransport", wie manche auch sagen.
Wie ist ein solcher Kanal aufgebaut?
Ein Kanal- oder Porenprotein ist ein Transmembranprotein (also ein Protein, das durch die gesamte Membran geht), das von einer in der Regel hydrophilen Pore durchzogen ist. Diese Pore ist mit polaren Aminosäuren ausgekleidet, so dass hydrophile Moleküle wie H2O oder Ionen wie Na+ oder Cl- durch die Pore diffundieren können.
Der Transport durch ein Kanalprotein erfolgt mit sehr hoher Geschwindigkeit, im Extremfall bis zu 105 mal schneller als der Transport von Stoffen über ein Carrierprotein und natürlich noch viel schneller als die freie Diffusion durch die Lipid-Doppelschicht.
Gehen Sie zu dieser Seite, wenn Sie den Grundaufbau eines Ionenkanals auf praktische Weise erfahren möchten. Sie bauen hier ein Papiermodell eines aus sieben Helices bestehenden Ionenkanals.
Aquaporine
Eine besondere Klasse von Kanalproteinen sind die Aquaporine, die zum schnellen Transport von Wasser in die Zelle / aus der Zelle heraus dienen. Aquaporine kommen in den Zellmembranen von allen Lebewesen vor, auch in Prokaryoten. Schließlich besteht eine Zelle zu ca. 70% aus Wasser, und irgendwie muss das Wasser ja in die Zelle hineinkommen. Klar, es könnte durch einfache Diffusion die Lipid-Doppelschicht passieren, das ist durchaus möglich, auch mit "vernünftiger" Geschwindigkeit. Allerdings reicht diese Geschwindigkeit für viele Zellprozesse nicht aus. Durch Aquoporine wird die Diffusion durch die Lipid-Doppelschicht um den Faktor 10.000.000 beschleunigt.
Ionen können durch Aquaporine nicht hindurch, selbst wenn sie kleiner sein sollten als ein Wasser-Molekül. Durch eine geschickte Verteilung geladener Aminosäure-Reste innerhalb der hydrophilen Pore werden sowohl positiv wie auch negativ geladene Ionen abgewiesen.
Wenn Sie mehr über Aquaporine lesen möchten, gehen Sie bitte auf diese Lexikon-Seite.
Ionenkanäle
Ionenkanäle sind auf den schnellen Transport von Ionen quer durch die Membran spezialisiert. Es gibt recht unspezifische Ionenkanäle, die mehrere Sorten positiver oder negativer Ionen passieren lassen, und es gibt sehr spezifische Ionenkanäle, die nur Na+, K+, Cl-, Ca2+- oder Mg2+-Ionen durchlassen. Man kennt inzwischen mehr als 100 verschiedene Ionenkanäle [1], eine Nervenzelle kann bis zu 10 unterschiedliche Typen von Ionenkanälen besitzen. Auch Pflanzen und Prokaryoten besitzen Ionenkanäle in ihrer Zellmembran.
Ionenkanäle sind keine simplen, ständig offenen Poren, durch die die Ionen einfach in Richtung des Konzentrationsgefälles ein- oder ausströmen können. Die meisten Ionenkanäle sind immer nur für kurze Zeit geöffnet, meistens sind sie geschlossen, bis auf wenige Ausnahmen. Die sogenannten Sickerkanäle sind in der Tat ständig geöffnet.
Warum sind Ionenkanäle meistens geschlossen?
Das soll an einem einfachen Beispiel erklärt werden. Eine normale Tierzelle enthält in ihrem Zellplasma nur ganz wenige Natrium-Ionen, dafür aber eine hohe Konzentration von Kalium-Ionen. In dem Außenmedium, das die Zelle umgibt, ist es genau umgekehrt: Viele Natrium-Ionen, aber nur ganz wenige Kalium-Ionen. Natürlich befinden sich auch viele negativ geladenen Ionen im Außenmedium und in der Zelle, um die positiven Ladungen der Natrium- bzw. Kalium-Ionen auszugleichen. Schauen wir uns das am besten mal in einem Bild an:
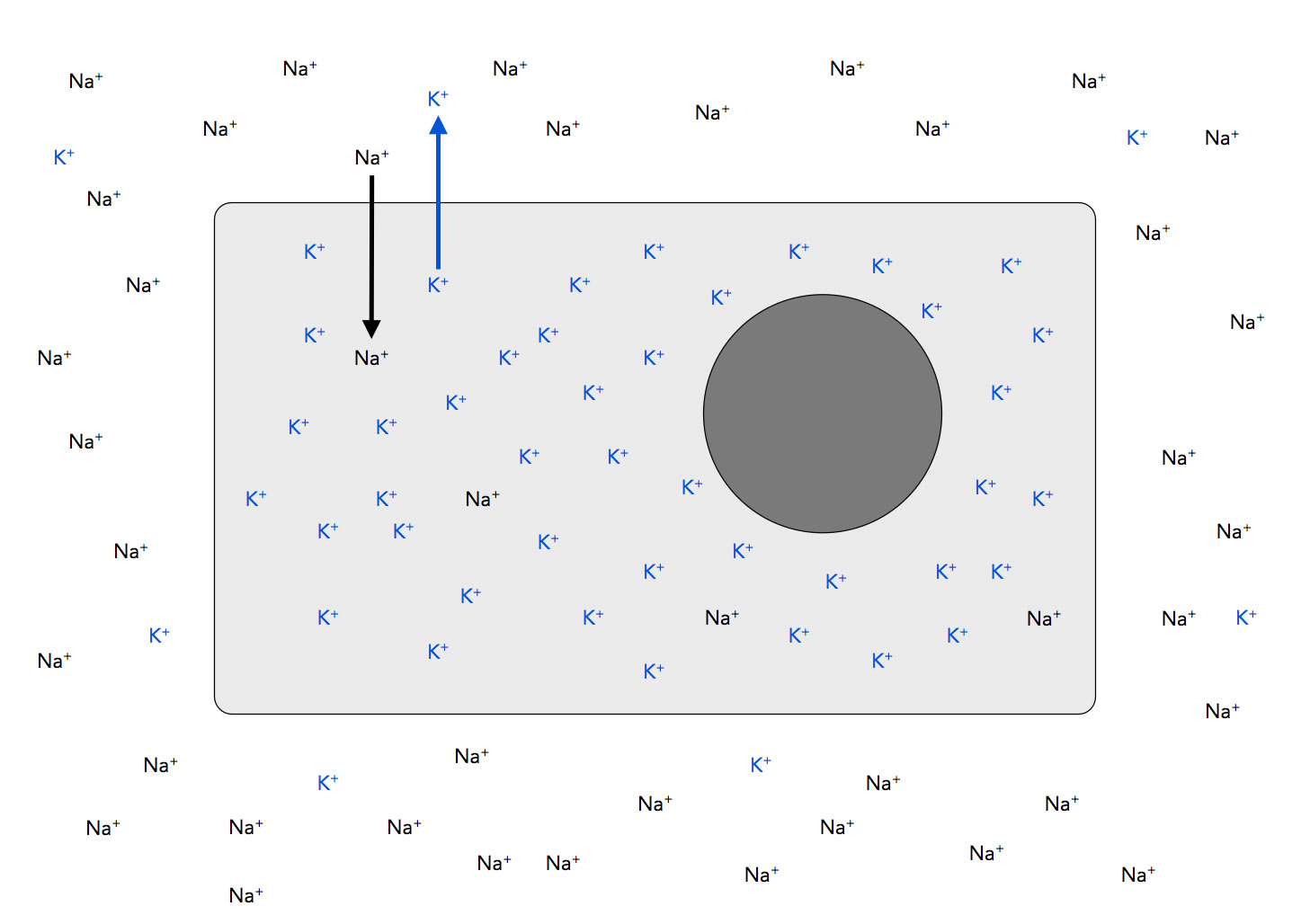
Konzentrationsverhältnisse der Kationen bei einer Tierzelle
Autor: Ulrich Helmich 2021, Lizenz: Public domain
Wären die Natrium- und Kaliumkanäle simple Poren, dann müsste jetzt eine starke Diffusion der Natrium-Ionen nach innen und der Kalium-Ionen nach außen einsetzen, so wie durch die beiden Pfeile in der Zeichnung angedeutet.
Die Zelle benötigt aber diese Konzentrationsunterschiede für ihre Funktion. Konzentrationsgradienten stellen eine Art gespeicherter Energie dar, die für viele Zwecke verwendet werden kann, zum Beispiel, um Nervenimpulse über lange Strecken am Axon einer Nervenzelle weiterzuleiten. Die vorhandenen Konzentrationsunterschiede dürfen also nicht einfach durch freie Diffusion zum Verschwinden gebracht werden. Die meisten Ionenkanäle sind daher in der Regel geschlossen und werden nur bei Bedarf geöffnet. Wenn beispielsweise am Axon einer Nervenzelle Aktionspotenziale zur nächsten Synapse weitergeleitet werden sollen, müssen ganz schnell ganz viele Natrium-Ionen in die Zelle fließen. Um das zu bewirken, öffnen sich Millionen von Natriumkanälen, die im Ruhezustand (also wenn keine Aktionspotenziale weitergeleitet werden sollen) geschlossen sind.
Wie wird denn das Öffnen und Schließen solcher Ionenkanäle gesteuert?
Ionenkanäle können auf drei verschiedene Weisen gesteuert werden
- Durch Liganden (meist kleinere Moleküle)
- Durch Veränderung der Membranspannung
- Durch mechanische Kräfte
Diese drei Mechanismen werden im folgenden Abschnitt näher erläutert.
Steuerung von Ionenkanälen
Ligandengesteuerte Ionenkanäle
Solche Ionenkanäle muss man sich wie ein allosterisches Enzym vorstellen. Nur ist das aktive Zentrum diesmal die Pore, durch die ein Ion in Richtung der niedrigeren Konzentration diffundieren kann. Neben dieser Pore besitzt ein solcher Ionenkanal noch eine Art allosterisches Zentrum, in die sich ein organisches Molekül nach dem Schlüssel-Schloss-Prinzip hineinsetzen kann. Sobald das der Fall ist, wenn also die Rezeptorstelle des Ionenkanals besetzt ist, öffnet sich der Kanal - oder er schließt sich, je nachdem, welche Aufgabe der Kanal zu erfüllen hat.
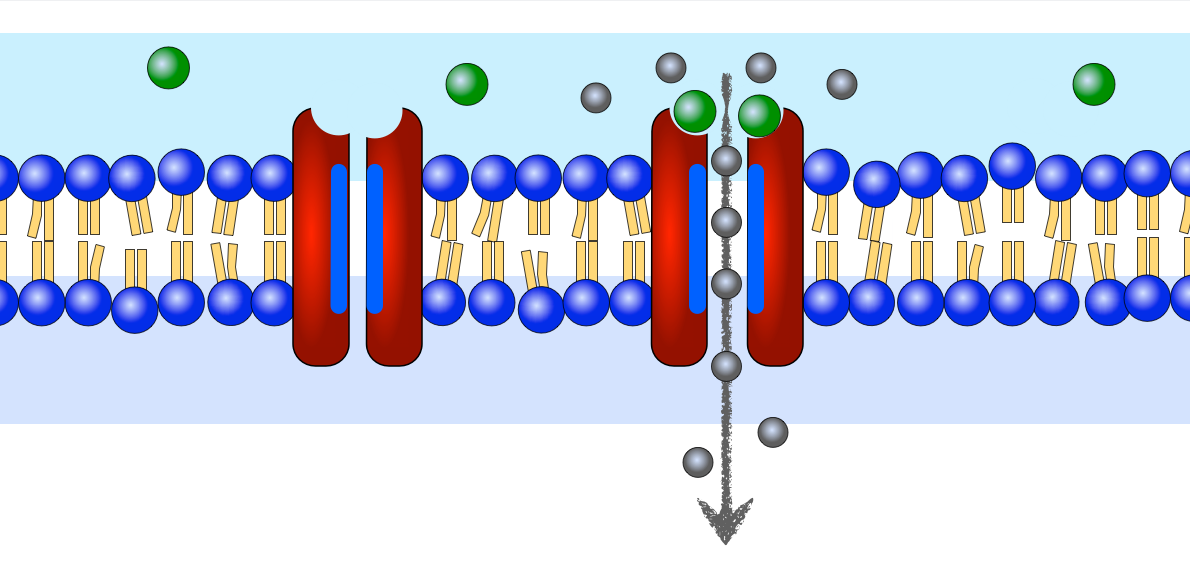
Ein ligandengesteuerter Ionenkanal
Autor: Ulrich Helmich 2021, Lizenz: Public domain
In diesem Bild sehen wir einen ligandengesteuerten Ionenkanal. Der Kanal hat auf der einen Membranseite eine oder mehrere Rezeptorstellen für Liganden, die hier durch grüne Kugeln dargestellt werden. Solange die Rezeptorstellen unbesetzt sind, ist der Kanal geschlossen.
Setzen sich nun Liganden wie Neurotransmitter oder sekundäre Botenstoffe (z.B. cAMP) in die Rezeptoren, steigt die Öffnungs-Wahrscheinlickeit des Kanals auf ca. 90%, und die Ionen können mit dem Konzentrationsgefälle durch die Membran diffundieren, teils mit Spitengeschwindigkeiten von 30.000 Ionen pro Millisekunde [1]. Die Liganden sind aber sehr locker gebunden und können sich jederzeit wieder aus den Rezeptorstellen lösen, worauf sich der Kanal wieder schließt. Ist die Ligandenkonzentration einigermaßen hoch, kann man ein ständiges Öffnen und Schließen der Kanäle beobachten.
Ein ligandengesteuerter Ionenkanal zeichnet sich durch eine zweifache Spezifität aus: Erstens ist er hochspezifisch für den Liganden, der sich nach einem strengen Schlüssel-Schloss-Prinzip in die Rezeptorstelle(n) hineinsetzt. Zweitens ist er grob spezifisch für die Ionen, die seine Pore passieren können. Natrium-Kanäle lassen beispielsweise auch Kalium- oder Calcium-Ionen passieren, aber keine negativ geladenen Chlorid-Ionen.
Spannungsgesteuerte Ionenkanäle
Eine andere Art, wie Ionenkanäle reguliert werden können, geht über die Membranspannung. Durch die ungleiche Verteilung positiver und negativer Ionen kann man an jeder Zellmembran eine kleine Spannung im Millivoltbereich messen. Nervenzellen beispielsweise haben im Ruhezustand eine Spannung von ca. -70 mV, wobei das Innere der Zelle negativ geladen ist.
Es gibt nun Ionenkanäle, die ihren Öffnungszustand ändern, sobald sich die Membranspannung wesentlich ändert. Also nicht, wenn sie von -70 mV auf -60 mV steigt, aber vielleicht, wenn sie von -70 mV auf -30 mV oder sogar auf +10 mV steigt.
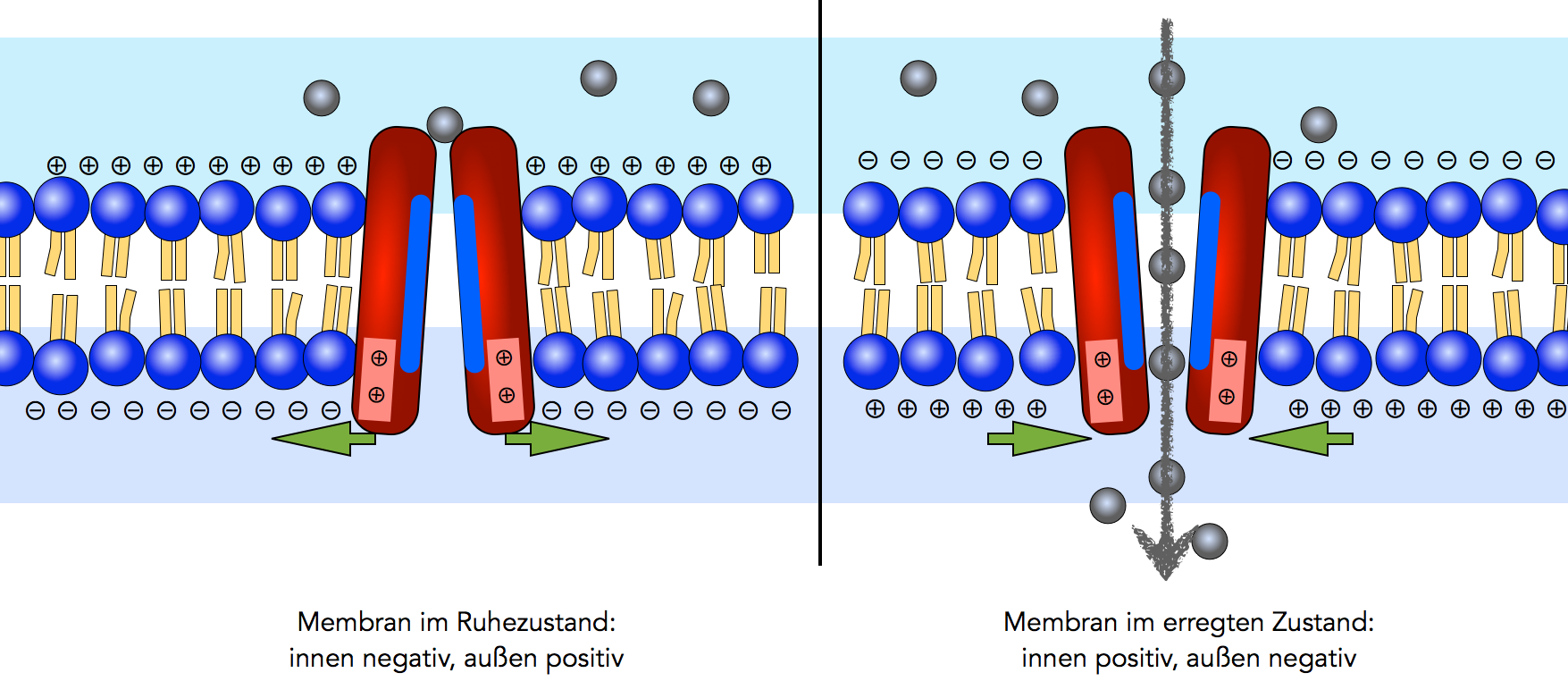
Ein spannungsgesteuerter Ionenkanal
Autor: Ulrich Helmich 2021, Lizenz: Public domain
Spannungsgesteuerte Ionenkanäle haben nicht nur eine hydrophile Pore, die Ionen passieren lässt (blau gezeichnet), sondern besitzen auch noch geschickt verteilte elektrische Ladungen (geladene Seitenketten von Aminosäuren), die auf Spannungsänderungen der Membran reagieren und den Kanal zum Öffnen oder zum Schließen veranlassen.
In der in der Abbildung gezeigten einfachen Modellvorstellung befinden sich zwei positive Ladungen in den cytoplasmatischen Bereichen des Kanalproteins. Das könnten zum Beispiel zwei positiv geladene Arginin- oder Lysin-Reste sein. Diese positiven Ladungen werden nun von der negativen Ladung angezogen, die normalerweise auf der Innenseite der Zellmembran herrscht. Dadurch wird die Konformation des Ionenkanals so geändert, dass die Pore geschlossen ist.
Kommt es nun zu einer Ladungsänderung, bei der die negative Ladung der Membraninnenseite schwächer wird oder sogar zu einer völligen Ladungsumkehr, so werden diese Bereiche des Kanalproteins nicht mehr so stark angezogen oder sogar abgestoßen. Die Konformation des Kanals ändert sich daraufhin, und die Ionen können passieren.
Mechanisch gesteuerte Ionenkanäle
Jedes Tier besitzt Sinne wie Hören, Tasten oder Fühlen. Verantwortlich dafür sind mechanisch gesteuerte Ionenkanäle. Sinneshaare, wie man sie zum Beispiel von Insekten kennt, berühren mit ihrer Wurzel über einen komplizierten Mechanismus Natrium-Kanäle bestimmter Nervenzellen. Verbiegt sich nun ein solches Sinneshaar, zum Beispiel durch den Fahrtwind eines vorbeifliegenden Beutetiers, so werden die beiden Hälften des Natrium-Kanals regelrecht auseinander gezogen. Dadurch können dann Natrium-Ionen in die Sinneszelle einströmen.
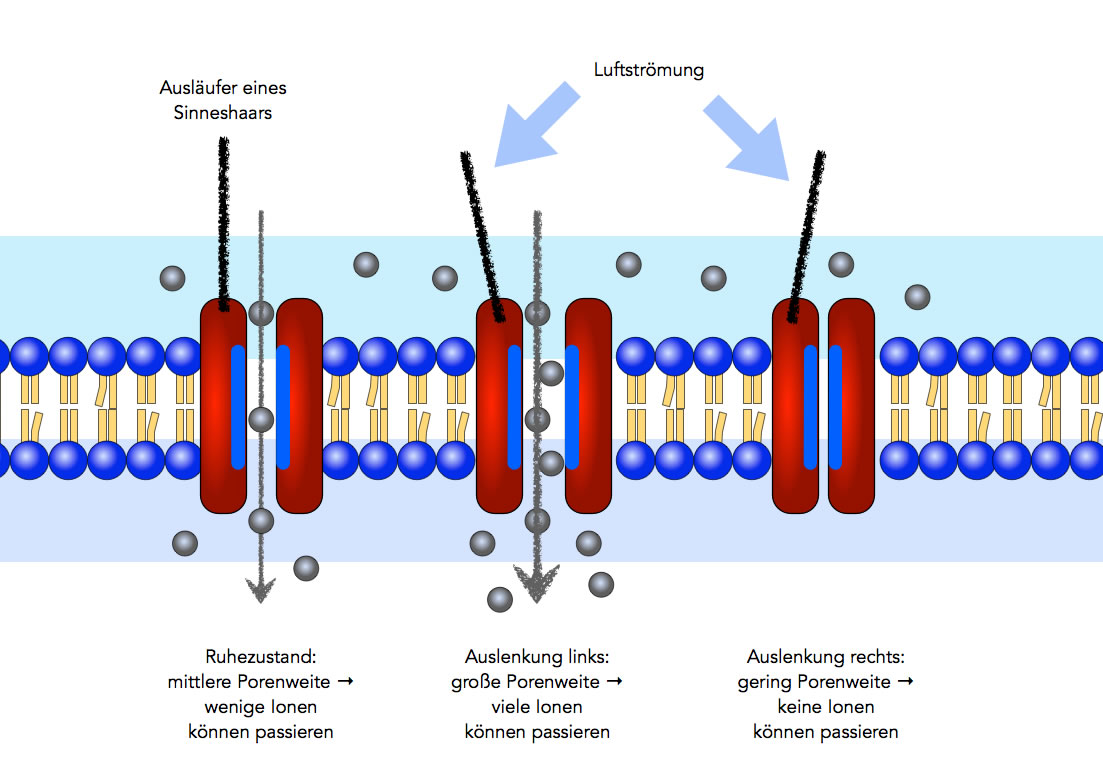
Ein mechanisch gesteuerter Ionenkanal
Autor: Ulrich Helmich 2021, Lizenz: Public domain
Verbiegt sich das Sinneshaar in die andere Richtung, werden die beiden Hälften des Kanals dagegen zusammengeschoben, es können dann gar keine Natrium-Ionen mehr in die Sinneszelle eindringen. Auf diese Weise kann das Tier dann sogar die Richtung ermitteln, aus der das Beuteinsekt angeflogen kam.
Die Diffusion durch Ionenkanäle
wird durch zwei Faktoren bestimmt
Bisher haben Sie gelernt, dass die Richtung und die Geschwindigkeit einer Diffusion von der Richtung und Größe des Konzentrationsgradienten abhängt, der ja ein chemisches Potenzial darstellt (chem. Potenzial = die Fähigkeit eines Konzentrationsgradienten, Arbeit zu leisten). Das ist so weit auch korrekt.
Bei Ionenkanälen, die elektrisch geladene Teilchen befördern, gibt es jedoch noch einen zweiten Faktor, der die Richtung und die Geschwindigkeit der Diffusion bestimmt, und zwar die Membranspannung, die ein elektrisches Potenzial bildet (Fähigkeit einer Spannung, Arbeit zu leisten).
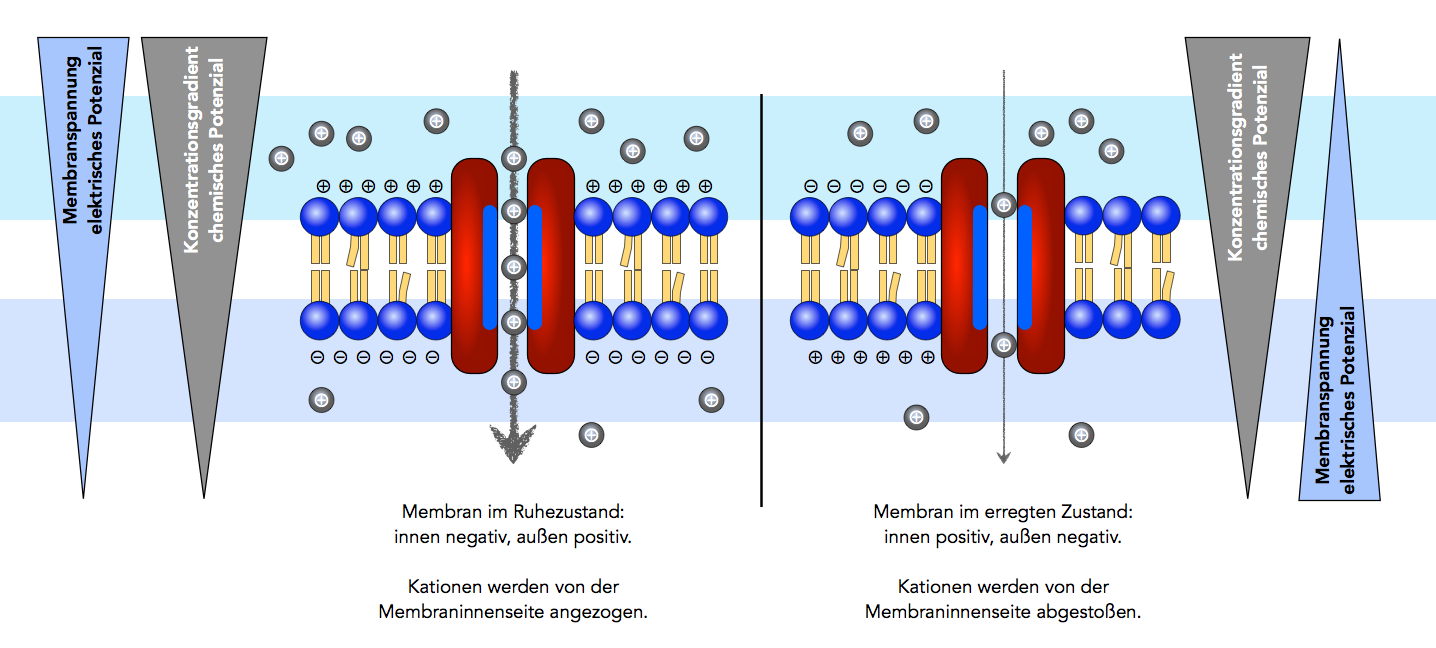
Die Diffusionsrichtung und -geschwindigkeit wird von zwei Faktoren bestimmt
Autor: Ulrich Helmich 2021, Lizenz: Public domain
Links in der Abbildung ist die Membraninnenseite negativ geladen - so wie sich das bei einer normalen Zellmembran im Ruhezustand auch "gehört". Natrium-Ionen sind im Außenmedium im Überschuss vorhanden und strömen aufgrund des Konzentrationsgradienten von außen nach innen. Zusätzlich werden die positiven Natrium-Ionen von der negativen Membraninnenseite angezogen und von der positiven Außenseite abgestoßen.
Chemisches Potenzial (Konzentrationsgradient) und elektrisches Potenzial (Membranspannung) weisen in die gleiche Richtung und addieren sich sozusagen. Die Folge ist ein intensiver Einstrom von Natrium-Ionen.
Rechts in der Abbildung ist die Membraninnenseite positiv geladen. Das ist beispielsweise der Fall, wenn eine Nervenzelle erregt ist und am Axon gerade Aktionspotenziale zu messen sind. Das chemische Potenzial ist immer noch eine starke Triebkraft für die Natrium-Ionen nach innen, das elektrische Potenzial zeigt jetzt aber in die Gegenrichtung. Die positive Membraninnenseite stößt die eindringenden Natrium-Ionen ab, und von der negativ geladenen Außenseite der Membran werden sie festgehalten.
Solange das elektrische Potenzial noch kleiner ist als das chemische, so wie auf der Abbildung rechts, strömen weiterhin Natrium-Ionen in die Zelle, aber mit stark verminderter Geschwindigkeit. Sollte das elektrische Potenzial einmal genau so stark sein wie das chemische, sollte also die Membranspannung den Konzentrationsgradienten kompensieren, dann strömen im Endeffekt keine Natrium-Ionen mehr in die Zelle. Es herrscht dann ein sogenanntes elektrochemisches Gleichgewicht: Pro Zeiteinheit strömen genau so viele Natrium-Ionen in die Zelle hinein wie aus ihr heraus strömen.
Sollte das elektrische Potenzial sogar größer sein als das chemische, strömen die Natrium-Ionen tatsächlich von innen nach außen, obwohl sich außen mehr Natrium-Ionen befinden als innen.
Seiten für fortgeschrittene Leute
Auf dieser Lexikonseite finden Sie eine ausführliche Darstellung der Funktionsweise des bakteriellen Kalium-Kanals. Dies war der erste Ionenkanal, dessen Funktionsweise gründlich untersucht wurde.
➥Natriumkanal, spannungsgesteuert
Auf dieser Lexikonseite finden Sie eine ausführliche Darstellung der Funktionsweise eines spannungsgesteuerten Natrium-Kanals.
Eine Seite zum ligandengesteuerten Natriumkanal der motorischen Endplatte ist in Vorbereitung!
Quellen:
- Alberts, Bruce et al. Molekularbiologie der Zelle, 6. Auflage, Weinheim 2017.
- Berg, Tymoczko, Gatto jr., Stryer: Stryer Biochemie, 8. Auflage, Springer Berlin Heidelberg 2018.