8.1 Pyrazol und Imidazol

Pyrazol und Imidazol
Autor: Ulrich Helmich 01/2024, Lizenz: Public domain
Beide Verbindungen sind aromatisch, weil eines der beiden N-Atome sein freies Elektronenpaar dem pi-System zur Verfügung stellt, so dass die (4n+2)-Regel mit sechs pi-Elektronen erfüllt wird. Das andere N-Atom hat sein freies Elektronenpaar in einem sp2-Orbital "nach außen" gerichtet, dieses Elektronenpaar verleiht beiden Verbindungen die Eigenschaften einer Lewis-Base.
Imidazol
Gleichzeitig ist Imidazol aber auch eine (gar nicht mal so schwache) Säure, wie man auf folgendem Bild gut sieht:

Das Säure-Base-Verhalten von Imidazol
Autor: Ulrich Helmich 01/2024, Lizenz: Public domain
Nimmt das Imidazol-Molekül als Brönsted-Base ein Proton auf, entsteht das Imidazol-Kation, das in zwei Grenzstrukturen vorliegt und daher recht stabil ist.
Gibt das Imidazol-Molekül dagegen ein Proton ab, bildet sich das Imidazol-Anion. Auch dieses Ion wird durch zwei Grenzstrukturen stabilisiert.
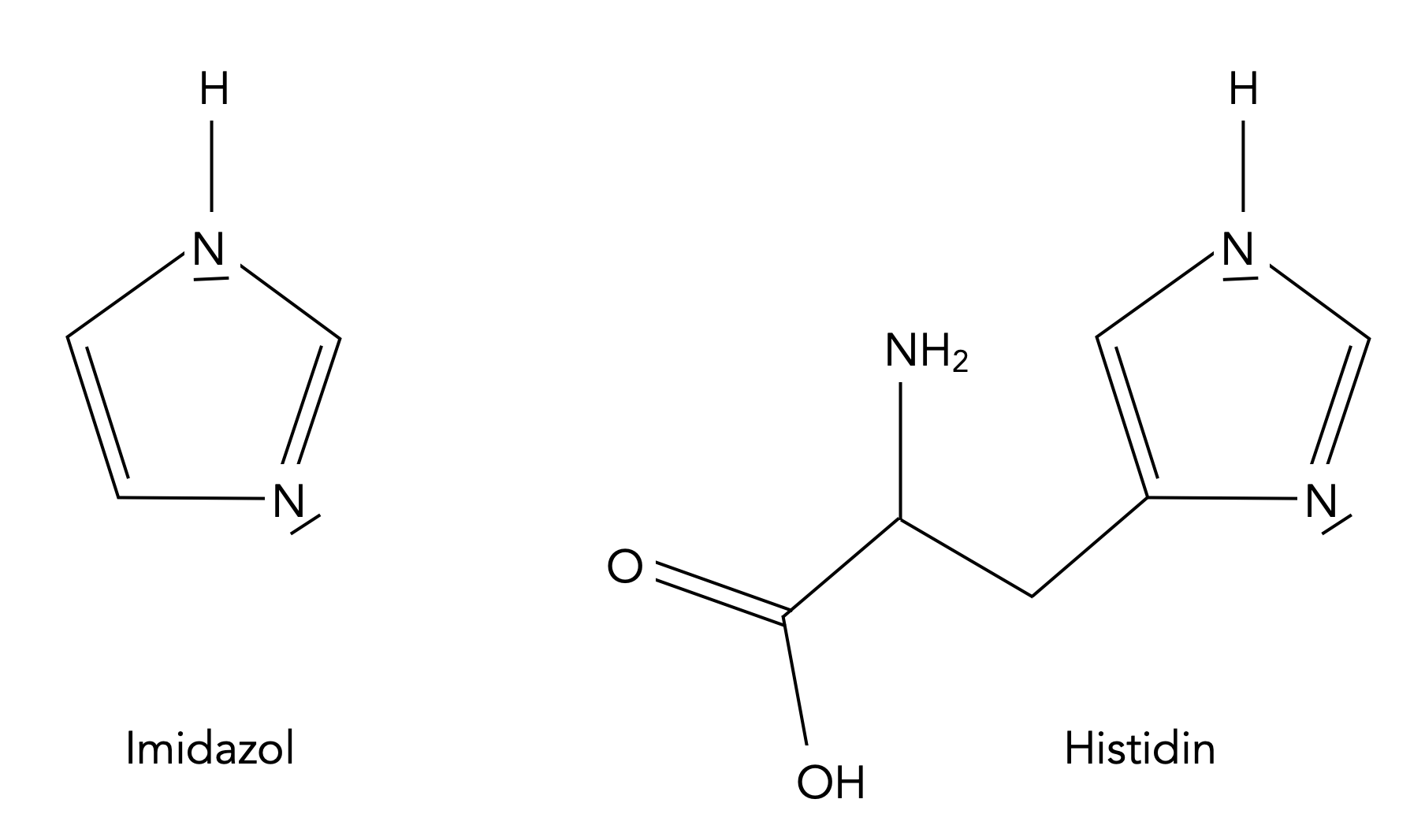
Imidazol ist ein Bestandteil der Aminosäure Histidin
Autor: Ulrich Helmich 01/2024, Lizenz: Public domain
Die Natur macht sich die ampholytische Eigenschaft von Imidazol zu Nutze wie wir am Beispiel der Aminosäure Histidin sehen, die einen Imidazol-Baustein enthält. Die Histidin-Seitengruppen von Proteinen können daher Protonen sowohl aufnehmen wie auch abgeben und können dann positiv bzw. negativ geladen sein.
Weitere Einzelheiten zu Imidazol finden Sie auf der entsprechenden Seite im Chemie-Lexikon dieser Homepage.
Für Mediziner
"The substituted imidazole derivatives are valuable in treatment of many systemic fungal infections. Imidazoles belong to the class of azole antifungals, which includes ketoconazole, miconazole, and clotrimazole." [6]
Pyrazol
Pyrazol ist der zweite fünfgliedrige Heteroaromat mit zwei Stickstoff-Atomen. Auf diese Verbindung müssen wir hier nicht besonders eingehen, weil sie fast die gleichen chemischen und physikalischen Eigenschaften hat wie Imidazol.
Für Mediziner
"In medicine, derivatives of pyrazole are widely used, including celecoxib and similar COX-2 inhibitors, zaleplon, betazole, and CDPPB" [7]
8.2 Triazole
Fünfgliedrige Heterocyclen mit drei N-Atomen werden als Triazole bezeichnet. Ein N-Atom der Triazole ist ähnlich wie beim Pyrrol mit einem H-Atom verbunden und stellt sein freies Elektronenpaar dem aromatischen System zur Verfügung. Die beiden anderen N-Atome sind genau wie beim Pyridin auch sp2-hybridisiert, stellen aber ihr freies Elektronenpaar nicht dem aromatischen System zur Verfügung, sondern haben ein doppelt besetztes sp2-Orbital "nach außen" gerichtet (im folgenden Bild blau gezeichnet):

1,2,3- und 1,2,4-Trioazol und ihre beiden Tautomere
Autor: Ulrich Helmich 01/2024, Lizenz: Public domain
Je nach Stellung der drei N-Atome unterscheidet man 1,2,3-Triazol und 1,2,4-Triazol. Von jeder dieser beiden Formen gibt es noch ein Tautomer, bei dem das H-Atom an einem anderen N-Atom sitzt.
Bei dieser Tautomerie handelt es sich also nicht um zwei Grenzstrukturen, sondern es muss tatsächlich ein H-Atom von einem N-Atom zum nächsten "wandern". Beide Tautomere befinden sich in einem Gleichgewicht.
Für Mediziner
Von den beiden Triazolen ist das 1,2,4-Triazol das Wichtigere, zumindest aus medizinischer Sicht. 1,2,4-Triazol ist nämlich "der Grundstoff für moderne Fungizide", also für Medikamente, die gegen Pilzerkrankungen helfen. Fluconazol von Pfizer enthält beispielsweise zwei dieser Triazol-Einheiten [3].
8.3 Tetrazole
Es gibt nur einen fünfgliedrigen Heterocyclen mit vier N-Atomen und einem einzigen C-Atom, dieser wird als Tetrazol bezeichnet. Die Derivate dieser Verbindung werden dann allgemein Tetrazole genannt.
Ähnlich wie die Triazole sind Tetrazole Lewis-Basen, können also beispielsweise Protonen aufnehmen. Im Gegensatz zu den Triazolen sind Tetrazole aber recht starke Säuren, der pKS-Wert liegt bei5, für organische Säuren ist das schon sehr hoch. Das Tetrazol-Anion, das nach Abgabe des Protons zurück bleibt, ist sehr stabil, da die negative Ladung über alle vier N-Atome delokalisiert ist.
Für Mediziner
Indometacin, ein Wirkstoff gegen Arthritis, enthält eine COOH-Gruppe. Diese kann leicht und ohne Verlust der Wirkung gegen eine Tetrazol-Gruppe ausgetauscht werden [3].
Quellen:
- VollhardT, Schore: Organische Chemie. 6. Auflage, Weinheim 2020.
- Morrison, Boyd, Bhattacharjee: Organic Chemistry. 7. Auflage, Dorling Kindersley 2011.
- J. Clayden, N. Greeves, S. Warren: Organische Chemie. Berlin 2013.
- Buddrus, Schmidt, Grundlagen der Organischen Chemie, 5. Auflage, De Gruyter-Verlag 2014.
- Houben-Weyl, Methoden der Organischen Chemie, Band Hetarenes I, Part 1, 4. Auflage, Stuttgart 1994.
- engl. Wikipedia, Artikel "Imidazole"
- engl. Wikipedia, Artikel "Pyrazole"
Seitenanfang -
Weiter mit Indol...