Struktur
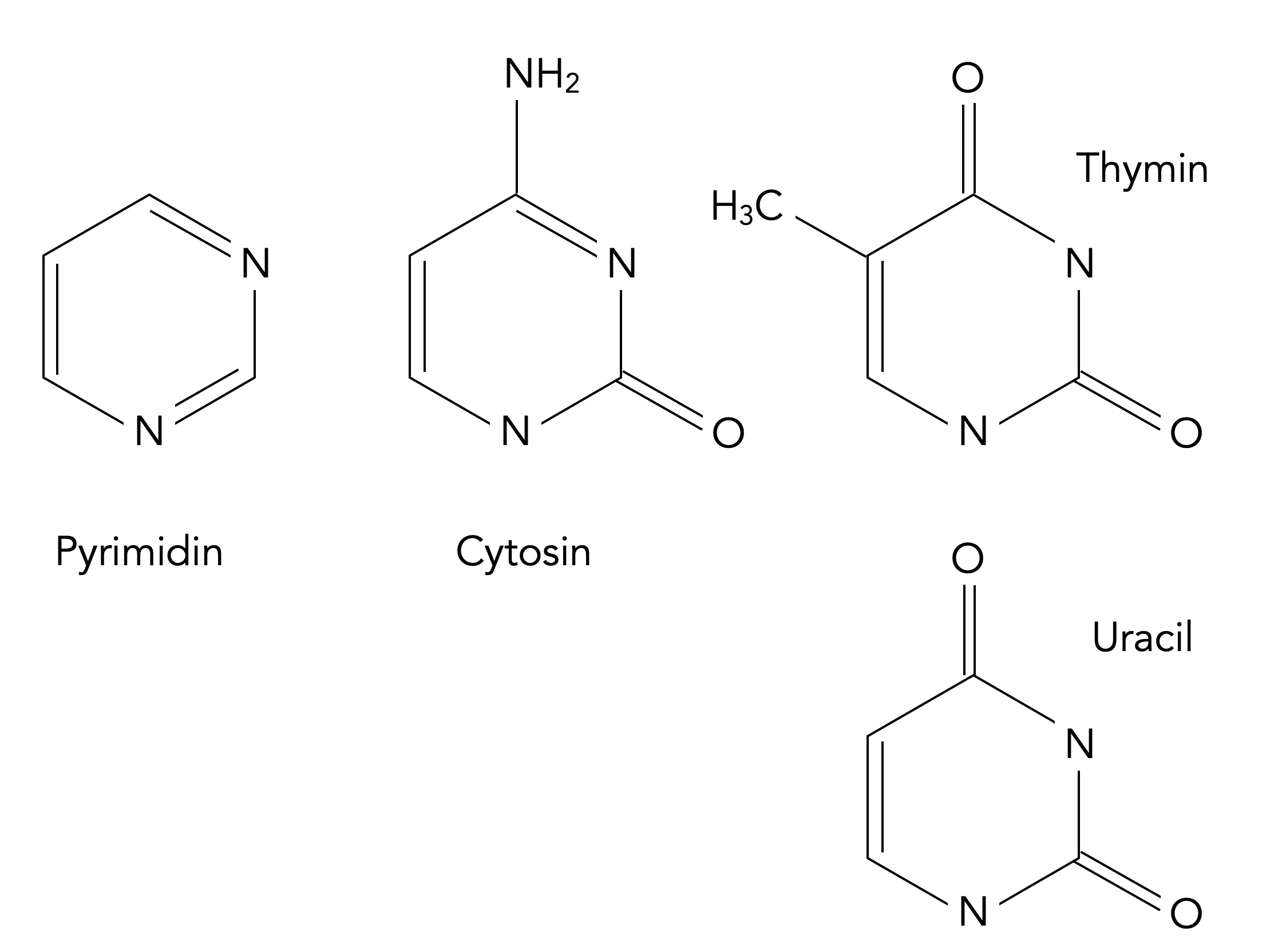
Pyrimidin und die drei Pyrimidin-Basen der DNA bzw. RNA
Autor: Ulrich Helmich 05/2023, Lizenz: CC BY-NC-SA 4.0
Das Pyrimidin-Molekül hat starke Ähnlichkeit mit dem Pyridin-Molekül, allerdings befindet sich ein zusätzliches zweites Stickstoff-Atom in dem Benzolring.
Mit seinen drei konjugierten Doppelbindungen und seiner planaren Ringstruktur erfüllt Pyrimidin die Hückel-Regel und ist daher aromatisch.
Diese wichtige Regel wurde von Erich Hückel (1896-1980) um 1930 aufgestellt. Mit dieser Regel kann man beurteilen, ob eine cyclische Verbindung mit Doppelbindungen aromatisch ist oder nicht.
Biologische Bedeutung
Die biologische Bedeutung von Pyrimidin geht schon aus der Abbildung hervor. Pyrimidin ist quasi die "Urmutter" aller Pyrimidin-Basen: Cytosin und Thymin sind DNA-Basen, während Uracil eine RNA-Base ist.
Außerdem ist Pyrimidin ein Bestandteil des Vitamins B1.
Eigenschaften
Pyrimidin ist ein farbloser kristalliner Feststoff mit einer Dichte von 1,016 g/cm3, einem Schmelzpunkt von 20 bis 22 ºC und einem Siedepunkt von 123 bis 124 ºC (Daten aus der Wikipedia).
Chemisch relevant ist, dass ähnlich wie beim Pyridin die freien Elektronenpaare der Stickstoff-Atome nicht zum aromatischen System gehören. Das hat den "Vorteil", dass sich eine Lewis-Säure an diese N-Atome anlagern kann, ohne den aromatischen Charakter des Pyrimidins aufzuheben.
Elektrophile Angriffe finden fast nur auf die N-Atome statt. Durch die -I-Effekte der beiden N-Atome ist die Elektronendichte im Ring stark verringert, und die C-Atome können fast nicht mehr elektrophil angegriffen werden. Nucleophile Substitutionen werden durch die beiden elektronenziehenden N-Atome dagegen wahrscheinlicher.
Weitere Einzelheiten zum Pyrimidin finden sich in diesem Wikipedia-Artikel (englisch; der deutsche Artikel ist etwas knapp gehalten).