Lernziele
Wenn Sie diese Seite durchgearbeitet haben, sollten Sie wissen
- wie man eine Apparatur zur Titration einer Säure (oder Lauge) aufbaut und
- wie man diese Apparatur korrekt bedient.
Versuch
In meinem Chemie-Unterricht der Oberstufe lasse ich zunächst ein paar einfache Titrationsübungen als Schülerversuch durchführen. An unserer Schule werden ähnliche Versuche bereits in der Sekundarstufe I durchgeführt, daher sollten meine S. keine Probleme mit einer einfachen Titration haben.
Versuch 1
Bestimmung der Konzentration verschiedener saurer Lösungen
Aufbau:
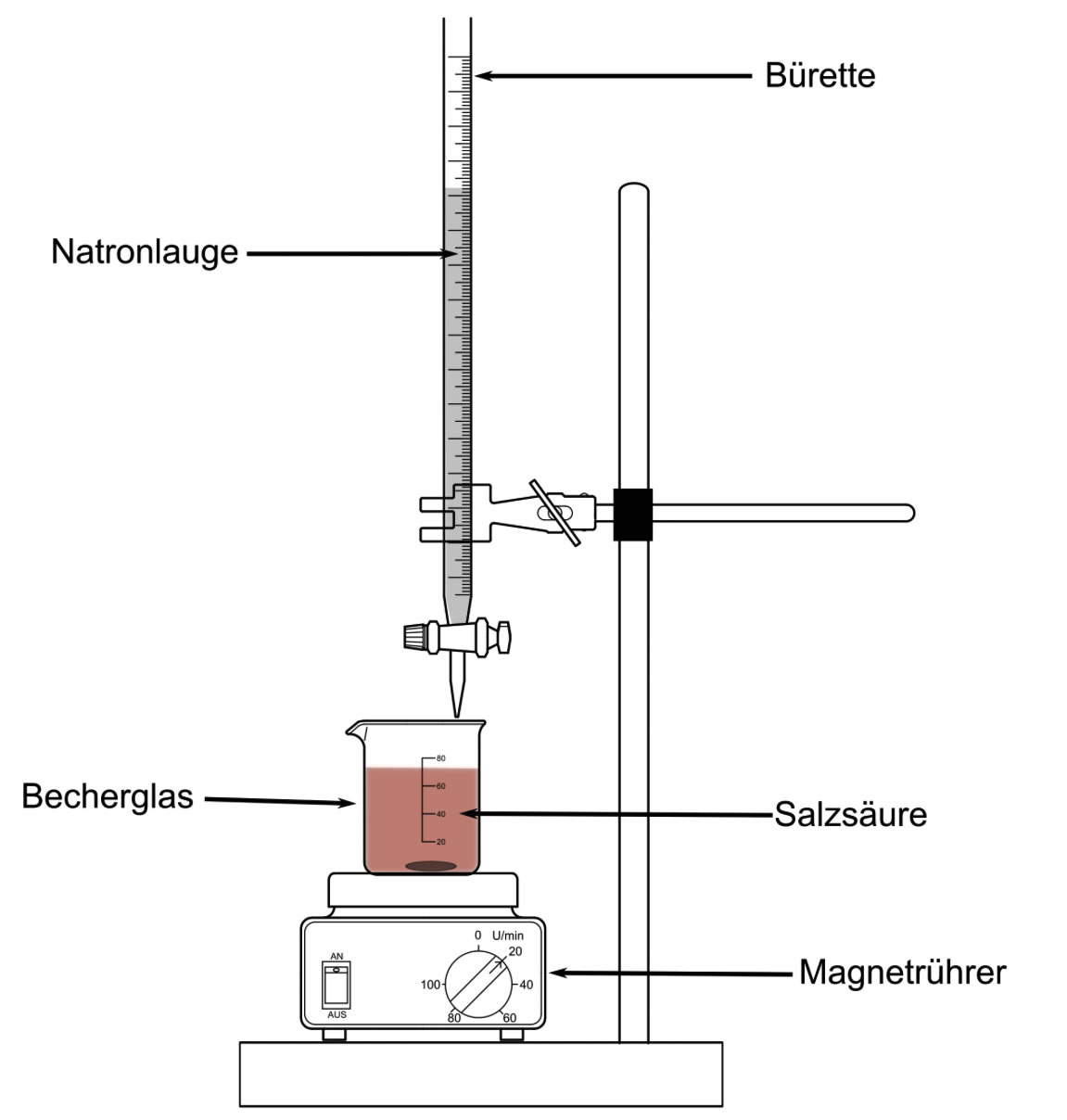
Eine typische Titrationsapparatur
Quelle: deutsche Wikipedia. Autor: Muskid.
Originalbild verändert von Ulrich Helmich am 31.08.2019 (pH-Sonde wurde entfernt, Säure wurde stattdessen mit Universalindidator versetzt).
This file is licensed under the Creative Commons Attribution-Share Alike 3.0 Unported license.
Durchführung:
Pipettieren Sie 1 ml Säure in eine Becherglas.
Verdünnen Sie die Säure mit 30 bis 50 ml destilliertem Wasser und fügen Sie einige Tropfen Universalindikator hinzu.
Titrieren Sie mit Natronlauge der Konzentration c(NaOH) = 0,1 mol/l bis zum Farbumschlag nach Grün und notieren Sie das Volumen der verbrauchten Lauge.
Als Säure verwenden Sie bitte
a) verdünnte Salzsäure (Konzentration 1 mol/l),
b) Batteriesäure (verdünnte Schwefelsäure, Konzentration nur der Lehrperson bekannt),
c) frisch gepressten Zitronensaft oder Lösung von Zitronensäure (Konzentration nur der Lehrperson bekannt).
Frage 1
Wieso ist es eigentlich völlig egal, mit welchem Wasser-Volumen die zu untersuchende Säure verdünnt wird?
Die Antwort finden Sie auf der nächsten Seite, nachdem wir besprochen haben, wie man die Konzentration von Säuren berechnet.
Frage 2
Warum wird für die erste Titration (a), die wir hier durchführen, eine Salzsäure mit bekannter Konzentration (1 mol/l) eingesetzt?
Die Antwort auf diese Frage finden Sie weiter unten auf dieser Seite.
Ausblick
Auf der nächsten Seite wollen wir - ausgehend von den Versuchsergebnissen - die Konzentration einer Säure berechnen.
Antwort auf Frage 2
In dem ersten Teilversuch soll gesichert werden, dass das Verfahren überhaupt korrekt funktioniert. Wenn wir 1 ml Salzsäure der Konzentration 1 mol/l mit Natronlauge der Konzentration 0,1 mol/l titrieren, sollten wir exakt 10 ml Natronlauge bis zum Umschlag des Indikators, also bis zur Neutralisation verbrauchen. Nicht mehr und nicht weniger. Falls wir mehr NaOH verbrauchen, war c(NaOH) geringer als 0,1 mol/l, und wenn wir weniger NaOH verbrauchen, war c(NaOH) höher als 0,1 mol/l.
Seitenanfang -
Weiter mit der Berechnung der Säure-Konzentration...