
Eliminierung (E1a und E1b - Mechanismus)
In diesem Video von Ramona Reinhart wird der E1-Mechanismus und seine Varianten sehr anschaulich erklärt.
Reaktionsmechanismus der Eliminierung
Schauen wir und die Dehydratisierung eines Alkohols jetzt mal etwas näher an. Wer sich von Ihnen dafür interessiert, wie der Versuch praktisch durchgeführt wird, kann ja noch einmal auf die entsprechende Seite zur Versuchsdurchführung gehen.
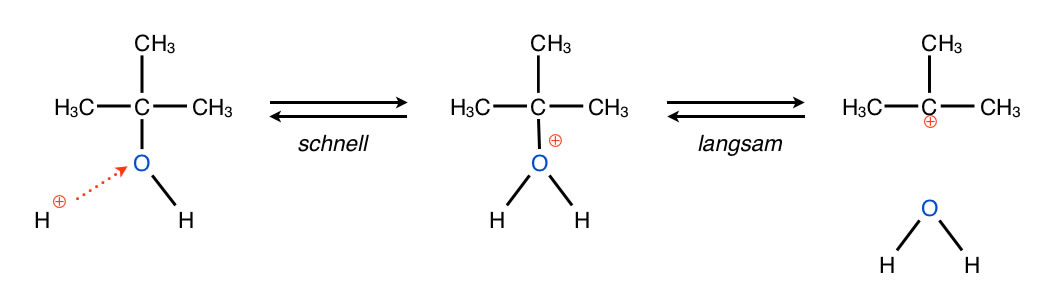
Bildung eines Carbenium-Ions
Autor: Ulrich Helmich 2017, Lizenz: Public domain.
Bei der Eliminierung müssen die OH-Gruppe und ein H-Atom aus dem Alkohol entfernt werden. Die OH-Gruppe ist allerdings eine sehr schlechte Abgangsgruppe (Nucleofug). Man kann aber "nachhelfen", indem man die Lösung ansäuert. Das haben wir bei dem Versuch durch die Zugabe von Schwefelsäure erreicht.
Versetzt man einen Alkohol mit einer Säure, so wird die OH-Gruppe protoniert. Die protonierte OH-Gruppe ist im Gegensatz zur "nackten" OH-Gruppe eine sehr gute Abgangsgruppe und kann leicht in Form eines Wasser-Moleküls abgespalten werden. Es bleibt ein Carbenium-Ion zurück. Das alles kennen wir bereits vom Schritt 1 des SN1-Mechanismus der Nucleophilen Substitution.
Der erste Schritt der E1-Eliminierung ist völlig identisch mit dem ersten Schritt der SN1-Substitution. Beide Reaktionen sind daher Konkurrenzreaktionen. Wenn Sie sich noch nicht mit der SN1-Reaktion beschäftigt haben, sollten Sie kurz auf diese Seite gehen.
Dieses Carbenium-Ion ist recht instabil und "versucht", seine positive Ladung irgendwie zu verlieren. Dazu gibt es zwei verschiedene Möglichkeiten.
- Anlagerung eines negativ geladenen Ions, zum Beispiel eines Bromid-Ions. Wird dieser Reaktionsweg eingeschlagen, so handelt es sich bei der Reaktion um den zweiten Schritt einer SN1-Reaktion.
- Abgabe eines Protons. Dies ist dann der Reaktionsweg der Eliminierung, bei der eine C=C-Doppelbindung entsteht, in diesem Falle bildet sich das Alken 2-Methyl-propen.
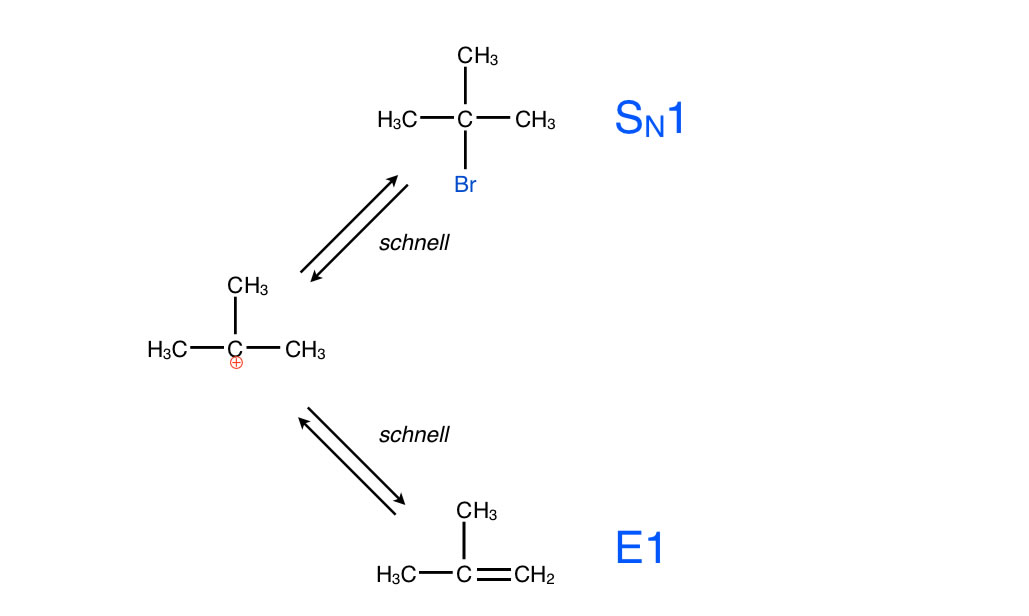
Die E1-Eliminierung als Konkurrenzreaktion zur SN1-Substitution
Autor: Ulrich Helmich 2017, Lizenz: Public domain.
Welcher der beiden Reaktionswege eingeschlagen wird, hängt natürlich von den genauen Reaktionsbedingungen ab. Sind beispielsweise keine Anionen im Reaktionsmedium vorhanden, so kann eigentlich nur der Weg der Eliminierung eingeschlagen werden. Eine weitere Konkurrenzreaktion werden wir noch weiter unten kennenlernen, die Ether-Bildung.
Die hier beschriebene Eliminierungsreaktion ist formal eine Umkehrung der säurekatalysierten Hydratisierung eines Alkens. Gehen Sie auf diese Seite, um mehr darüber zu erfahren.
Reaktionsgeschwindigkeit
Das Zwischenprodukt der Alkohol-Dehydratisierung hat entscheidenden Einfluss auf die Reaktionsgeschwindigkeit. Bekanntlich sind tertiäre Carbenium-Ionen besonders stabil, während primäre Carbenium-Ionen sehr instabil sind. Aus diesem Grund können tertiäre Alkohole besonders leicht dehydratisiert werden. In dem Chemie-Buch "Chemie heute SII" aus dem Schroedel-Verlag habe ich folgende Daten dazu gefunden: Die säurekatalysierte Dehydratisierung eines primären Alkohols erfordert Temperaturen von 200 ºC, die Dehydratisierung eines sekundären Alkohols 140 ºC, und die Dehydratisierung eines tertiären Alkohols gelingt bereits bei 80 ºC.
Etherbildung
Eben hatten wir gesehen, dass die SN1-Reaktion eine Konkurrenzreaktion zur E1-Eliminierung ist und umgekehrt. Aber auch dann, wenn kein Nucleophil in dem Reaktionsmedium anwensend ist, kann eine SN1-Reaktion stattfinden. Der Alkohol kann nämlich mit sich selbst reagieren. Bei niedrigeren Temperaturen reagiert das Carbenium-Ion mit einem weiteren Alkohol-Molekül als Nucleophil und es entsteht ein Ether-Molekül:
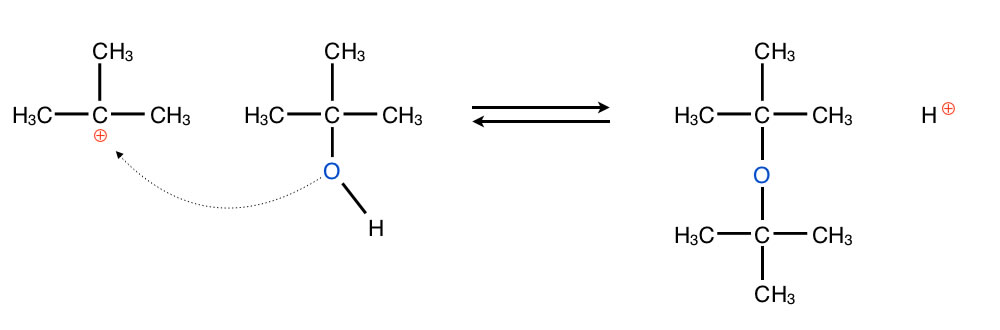
Die Etherbildung ist ebenfalls eine SN1-Reaktion
Autor: Ulrich Helmich 2017, Lizenz: Public domain.
E1-Eliminierung
Die E1-Eliminierung ist die Konkurrenzreaktion zur SN1-Substitution. Der erste und geschwindigkeitsbestimmende Schritt ist bei beiden Reaktionen gleich: In einer monomolekularen Reaktion wird ein Nucleofug abgespalten, und es bildet sich ein Carbenium-Ion als Zwischenprodukt.
Wenn sich dann ein Nucleophil an das Carbenium-Ion anlagert, haben wir es mit der SN1-Substitution zu tun. Spaltet sich dagegen ein Proton ab, wobei sich dann eine C=C-Doppelbindung bildet, liegt eine E1-Eliminierung vor.
Neben der E1-Eliminierung gibt es aber auch noch die E2-Eliminierung, die auf der nächsten Seite näher besprochen werden soll.
Abitur NRW
Im Zentralabitur NRW wird in einigen Aufgaben auf die Eliminierung als Konkurrenzreaktion zur SN1-Substitution eingegangen. Als Beispiel sei die Aufgabe von 2007 "Antiklopfmittel MTBE" genannt.
Insgesamt kommt das Stichwort "Eliminierung" in einer ganzen Reihe von Abituraufgaben vor, wie der folgende Screenshot einer Spotlight-Suche im Ordner "Abitur Chemie" zeigt:

Abituraufgaben NRW, in denen das Wort "Eliminierung" vorkommt
Autor: Ulrich Helmich 2017, Lizenz: Public domain.
Eine Suche nach "E1" oder E2" führte allerdings zu 0 Ergebnissen. Für das Chemie-Abitur in NRW reicht es offensichtlich, wenn man überhaupt weiß, dass es so etwas wie eine Eliminierung gibt. Nach welchem Mechanismus diese abläuft, scheint völlig egal zu sein.
Quellen:
- M. A. Fox, J. K. Whitesell: Organische Chemie - Grundlagen, Mechanismen, bioorganische Anwendungen. 1. Auflage, Heidelberg 1995.
- K. P. C. Vollhard, N.E. Schore: Organische Chemie. 6. Auflage, Weinheim 2020.
- J. Clayden, N. Greeves, S. Warren: Organische Chemie. Berlin 2013.
- R. T. Morrison, R. N. Boyd, S. K. Bhattacharjee: Organic Chemistry. 7. Auflage, Dorling Kindersley 2011.
- Reinhard Brückner, Reaktionsmechanismen, 3. Auflage, Springer-Verlag 2014.
- Organikum, 22. Auflage, Weinheim 2004.
- J. Falbe, M. Regitz (Herausgeber): Römpp Chemie Lexikon in 6 Bänden. 9. Auflage, Stuttgart, New York 1989-1992.