Struktur
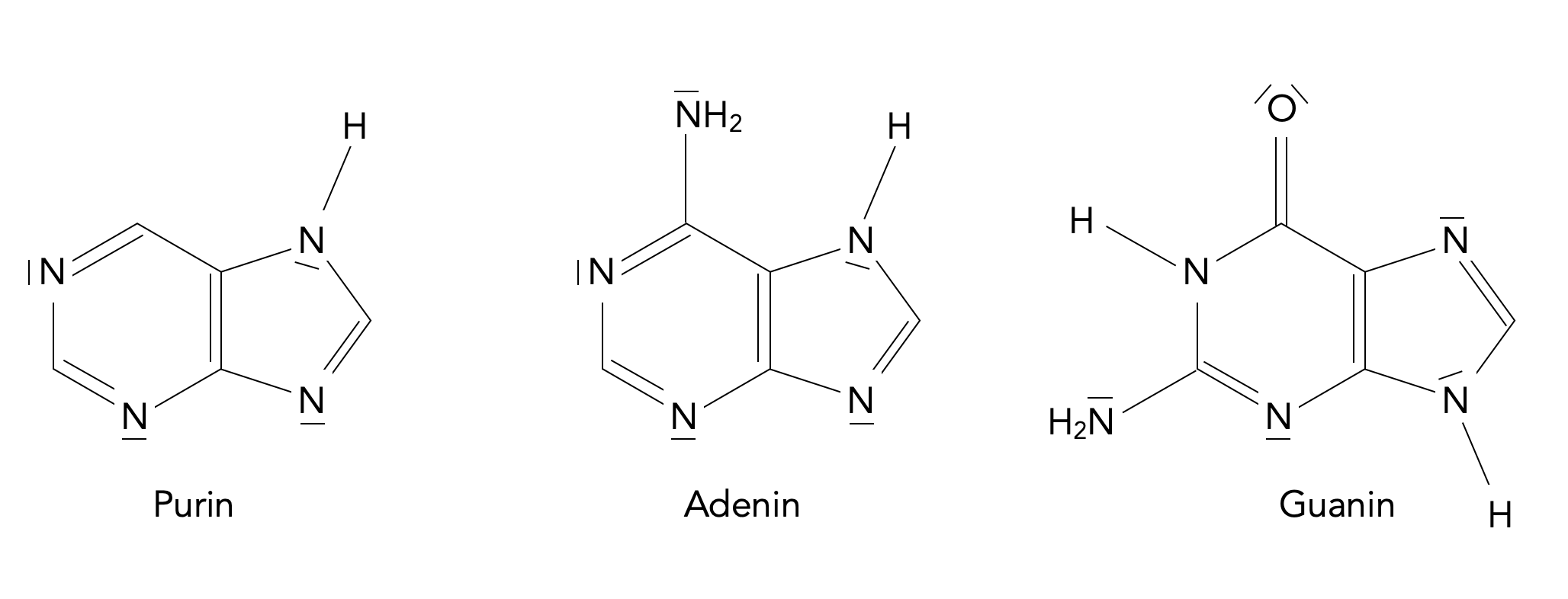
Purin und die beiden Purin-Basen der DNA bzw. RNA
Autor: Ulrich Helmich 05/2023, Lizenz: CC BY-NC-SA 4.0
Das Purin-Molekül setzt sich aus einem Pyrimidin- und einem Imidazol-Ring zusammen. Es handelt sich um ein kondensiertes Ringsystem. Insgesamt 10 pi-Elektronen (8 von den C-Atomen, 2 von dem einen N-Atom) erfüllen die (4n+2)-Regel von Hückel für n=2, Purin ist damit aromatisch.
Biologische Bedeutung
Die biologische Bedeutung von Purin geht schon aus der Abbildung hervor. Purin ist quasi die "Urmutter" aller Purin-Basen: Adenin und Guanin sind DNA- und RNA-Basen sowie Bestandteile weiterer Energieträger (ATP, GTP) sowie Coenzyme wie NAD oder NADP.
Eigenschaften
Purin ist ein farbloser kristalliner Feststoff mit einer Dichte von 1,22 g/cm3, einem Schmelzpunkt von 217 ºC. Weder die Wikipedia noch der Römpp geben einen Schmelzpunkt an, daher ist anzunehmen, dass sich Purin beim starken Erhitzen zersetzt.
Chemisch relevant ist, dass ähnlich wie beim Pyridin die freien Elektronenpaare der nicht mit einem H-Atom verbundenen N-Atome nicht zum aromatischen System gehören. Das hat den "Vorteil", dass sich eine Lewis-Säure an diese N-Atome anlagern kann, ohne den aromatischen Charakter des Purins aufzuheben.
Purin kann an den Stickstoff-Atomen von Elektrophilen und Lewis-Säuren angegriffen werden (zum Beispiel Protonierung), und die H-Atome an den C-Atomen der Ringe können elektrophil substituiert werden, Nitrierungen, Sulfonierungen, Bromierungen etc. sind damit problemlos möglich.
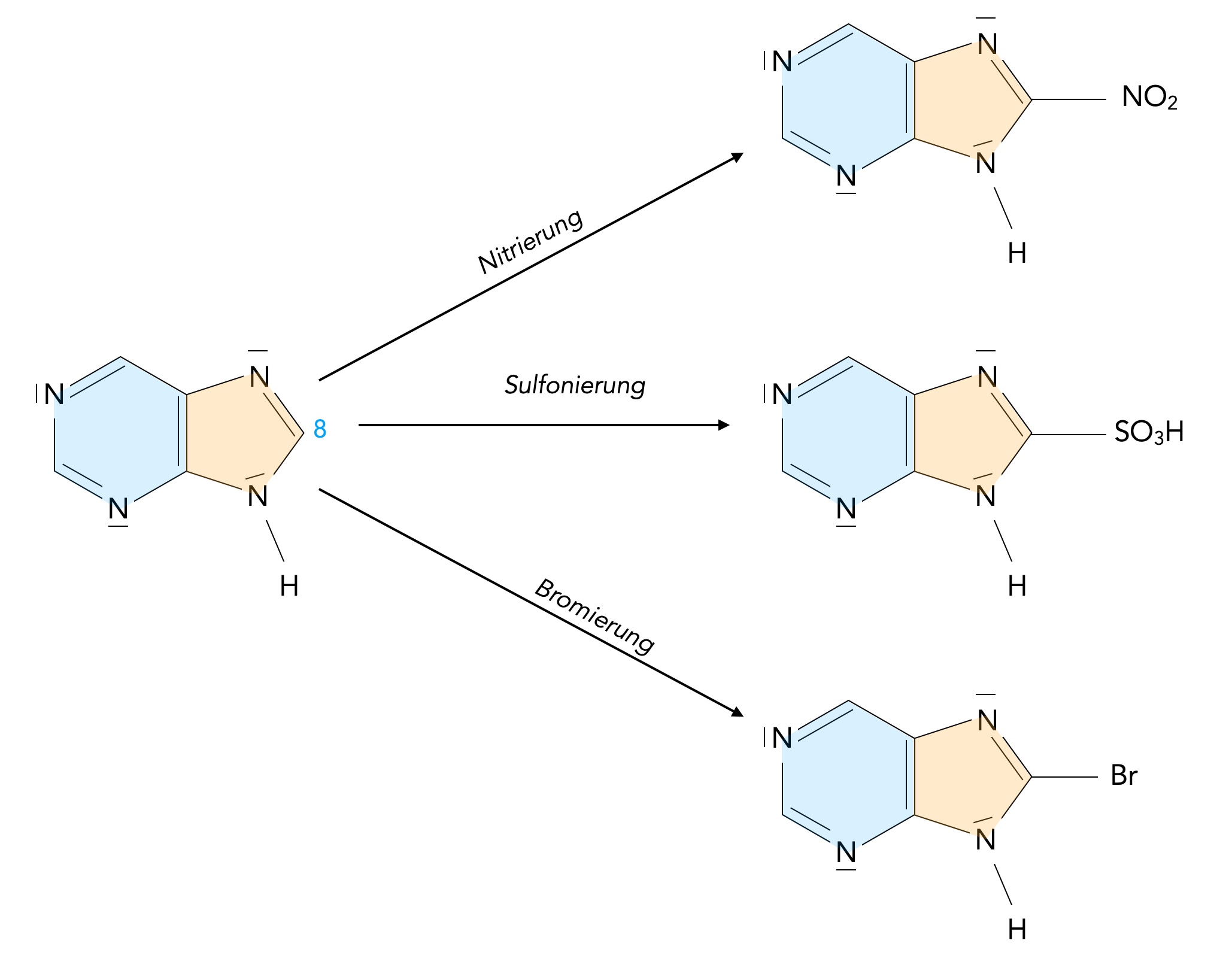
Nitrierung, Sulfonierung und Bromierung von Purin
Autor: Ulrich Helmich 01/2024, Lizenz: Public domain
Einen vertiefenden Artikel zum Purin und seinen Derivaten finden Sie in der Abteilung "Studienvorbereitung Organische Chemie" auf dieser Homepage.
Weitere Einzelheiten zum Purin finden sich in diesem Wikipedia-Artikel.