Synthese
Fluorescein ist ein wichtiger Triphenylmethan-Farbstoff, der leicht im Chemieunterricht hergestellt werden kann. Dazu werden ungefähr gleich große Mengen Phthalsäureanhydrid (oder Phthalsäure) und Resorcin mit ein paar Tropfen konz. Schwefelsäure in einem Reagenzglas gemischt und vorsichtig zum Schmelzen gebracht. Die Schmelze wird dann in ein großes Becherglas mit verdünnter Natronlauge (10%) gegossen, und man erlebt ein gelbgrün fluoreszierendes Farbwunder. Chemisch gesehen handelt es sich bei der Synthese von Phenolphthalein um eine Friedel-Crafts-Acylierung.
Schritt 1: Protonierung von Phthalsäureanhydrid
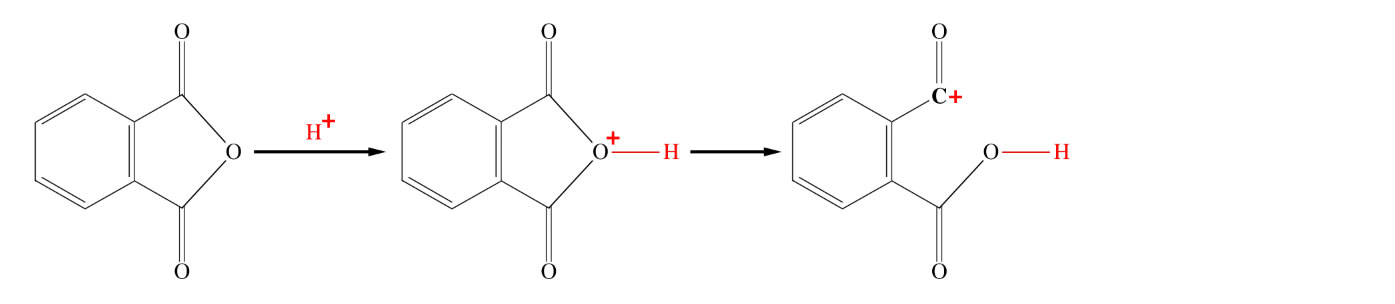
Protonierung von Phthalsäureanhydrid
Die Schwefelsäure spaltet ein Proton ab, mit dem dann das Edukt Phthalsäureanhydrid protoniert wird. Das Gleiche funktioniert übrigens auch mit der Phthalsäure selbst; es muss also nicht unbedingt das Anhydrid eingesetzt werden. Die hygroskopische konz. Schwefelsäure wandelt die Phthalsäure nämlich in Phthalsäureanhydrid um.
Sie können sich sicherlich schon denken, was im nächsten Schritt passiert.
Schritt 2: Elektrophile Substitution am Resorcin
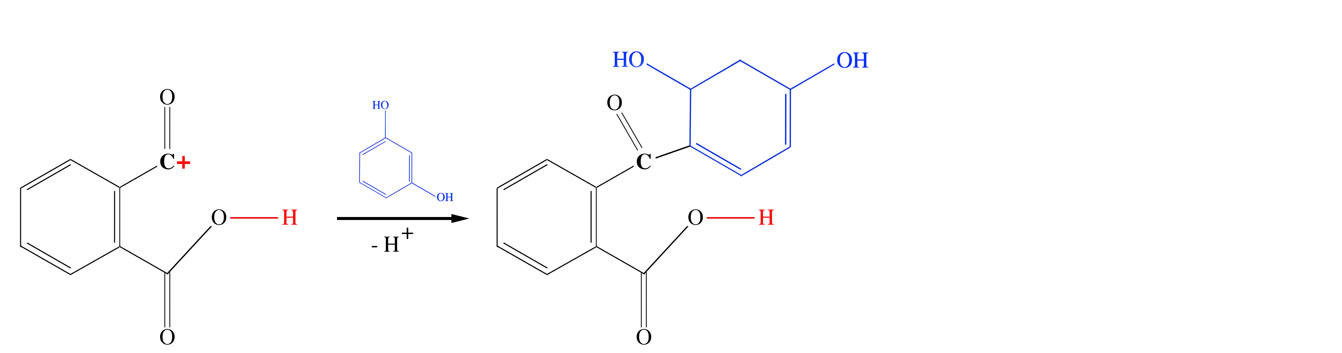
Elektrophile Substitution am Resorcin
Das entstandene Carbenium-Ion setzt sich in einem elektrophilen Substitutionsschritt an ein Resorcin-Molekül. Das obere Carbonyl-C-Atom im Zwischenprodukt ist jetzt mit zwei Benzolringen verbunden. Damit ein Triphenylmethan-Farbstoff entsteht, muss aber noch ein dritter Benzolring "angebaut" werden.
Schritt 3: Erneute Protonierung
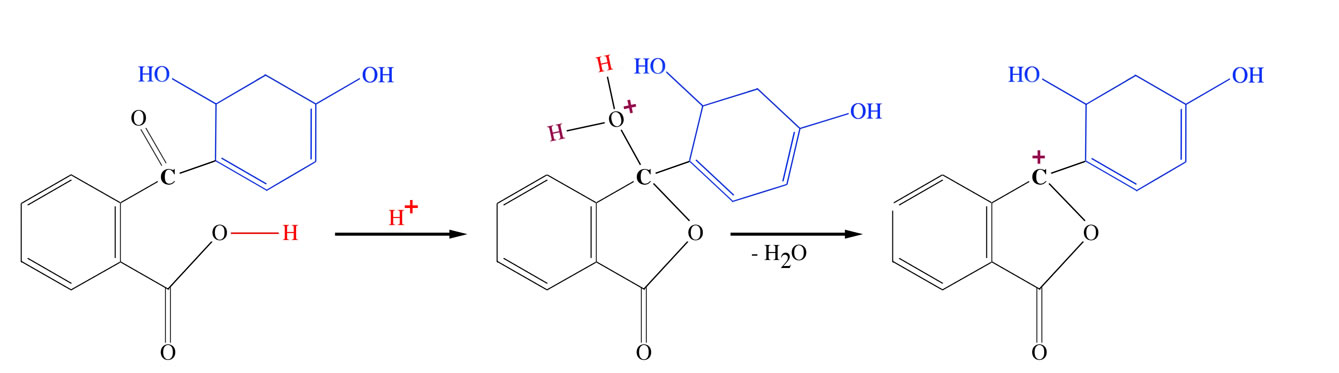
Erneute Protonierung und Wasserabspaltung
Ein weiteres Proton der konz. Schwefelsäure protoniert nun das Sauerstoff-Atom der oberen Carbonylgruppe, das so entstandene Wasser-Molekül wird nun abgespalten, übrig bleibt ein neues, größeres Carbenium-Ion mit zwei Benzolringen.
Schritt 4: Erneute Substitution
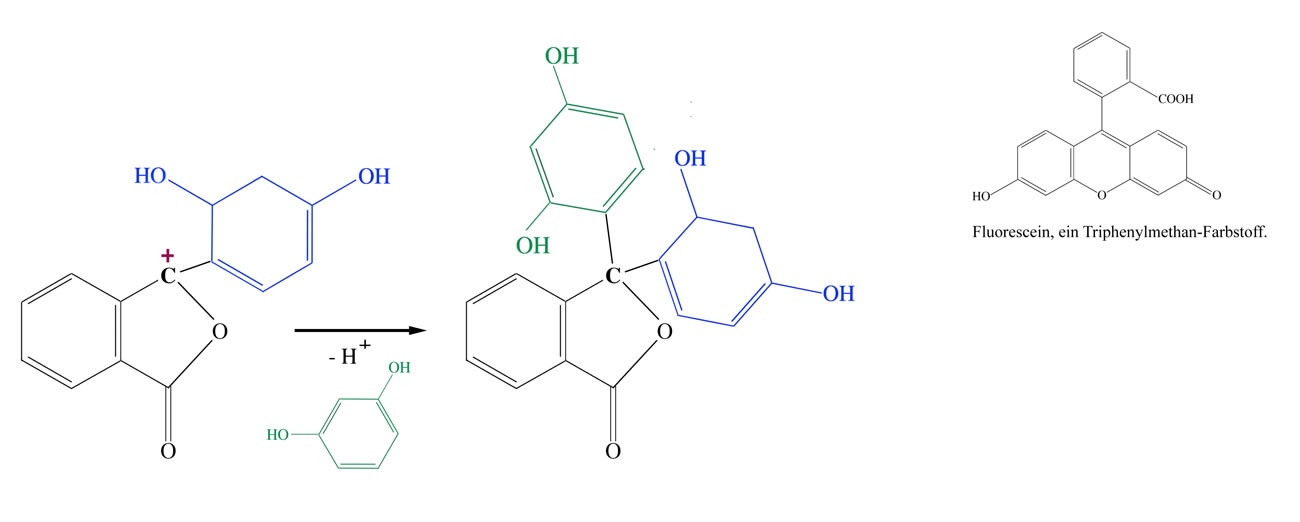
Die zweite elektrophile Substitution
Das Produkt dieses Schrittes ist ein Triphenylmethan-Derivat, das aber noch keine Farbstoffeigenschaften besitzt. Das mittlere C-Atom ist noch sp3-hybridisiert, das heißt, die delokalisierten Elektronen der drei Benzolringe haben noch keine Verbindung, sie sind nur innerhalb der einzelnen Benzolringe delokalisiert.
Schritt 5: Farbigkeit
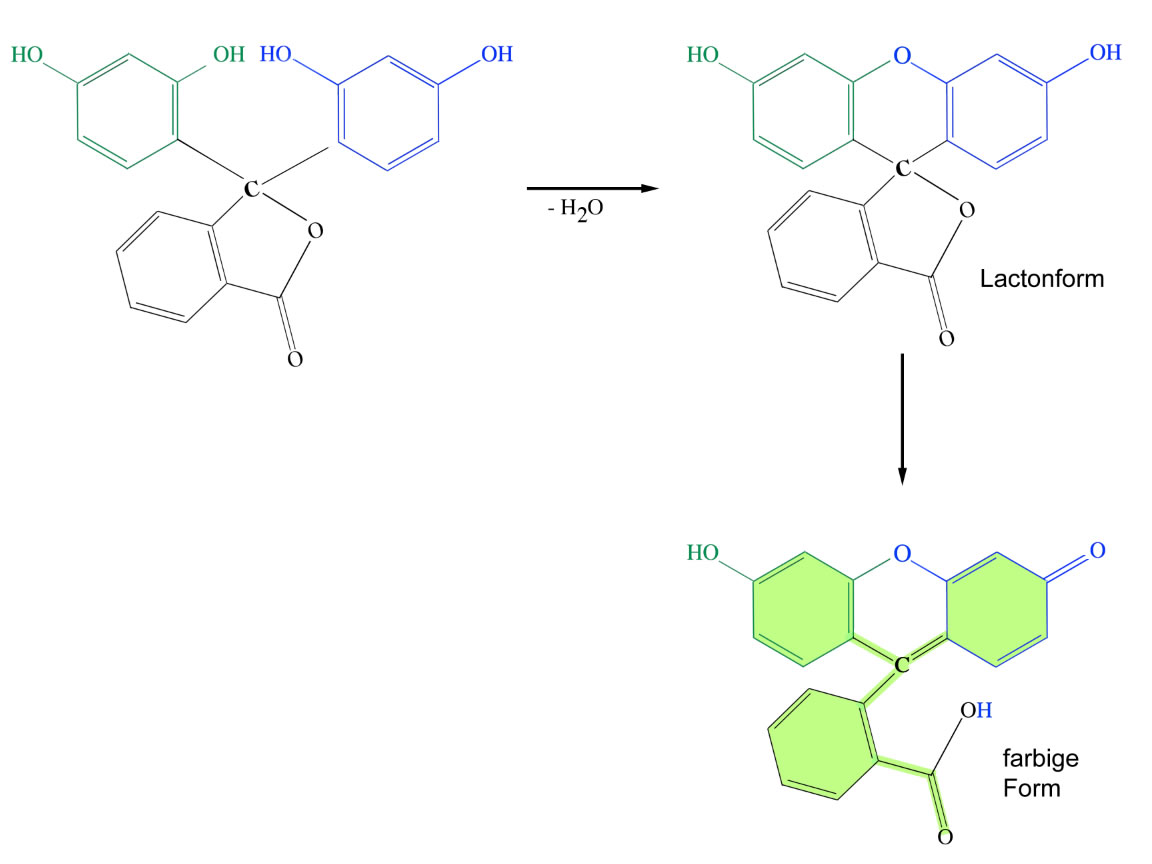
Die letzten beiden Schritte der Fluorescein-Synthese
Der vorletzte Schritt der Fluorescein-Synthese ist der Ringschluss. Die beiden Resorcin-Ringe kondensieren unter Wasserabspaltung zur sogenannten Lactonform. Diese lagert sich dann reversibel zur farbigen Form um.
In der Lactonform ist das zentrale C-Atom noch sp3-hybridisiert und stellt somit für die vielen delokalisierten Elektronen in den drei Benzolringen ein Hindernis dar. In der farbigen Form dagegen ist das Zentralatom sp2-hybridisiert, die vielen Elektronen könnten also im gesamten grün markierten Bereich frei "umher schwirren", wenn der "untere" Phenylring in der gleichen Ebene liegen würde wie der "obere" Xanthenring.
Leider ist das nicht der Fall, im Gegenteil, der Phenylring wird sterisch (und vielleicht auch elektrostatisch) von dem Xanthenring abgestoßen und dreht sich um ca. 90 Grad. Die pz-Orbitale des Phenylrings können also nicht mit den pz-Orbitalen des Xanthenrings überlappen, die "farbgebenden" pi-Elektronen befinden sich also nur in dem "oberen" Xanthenring.
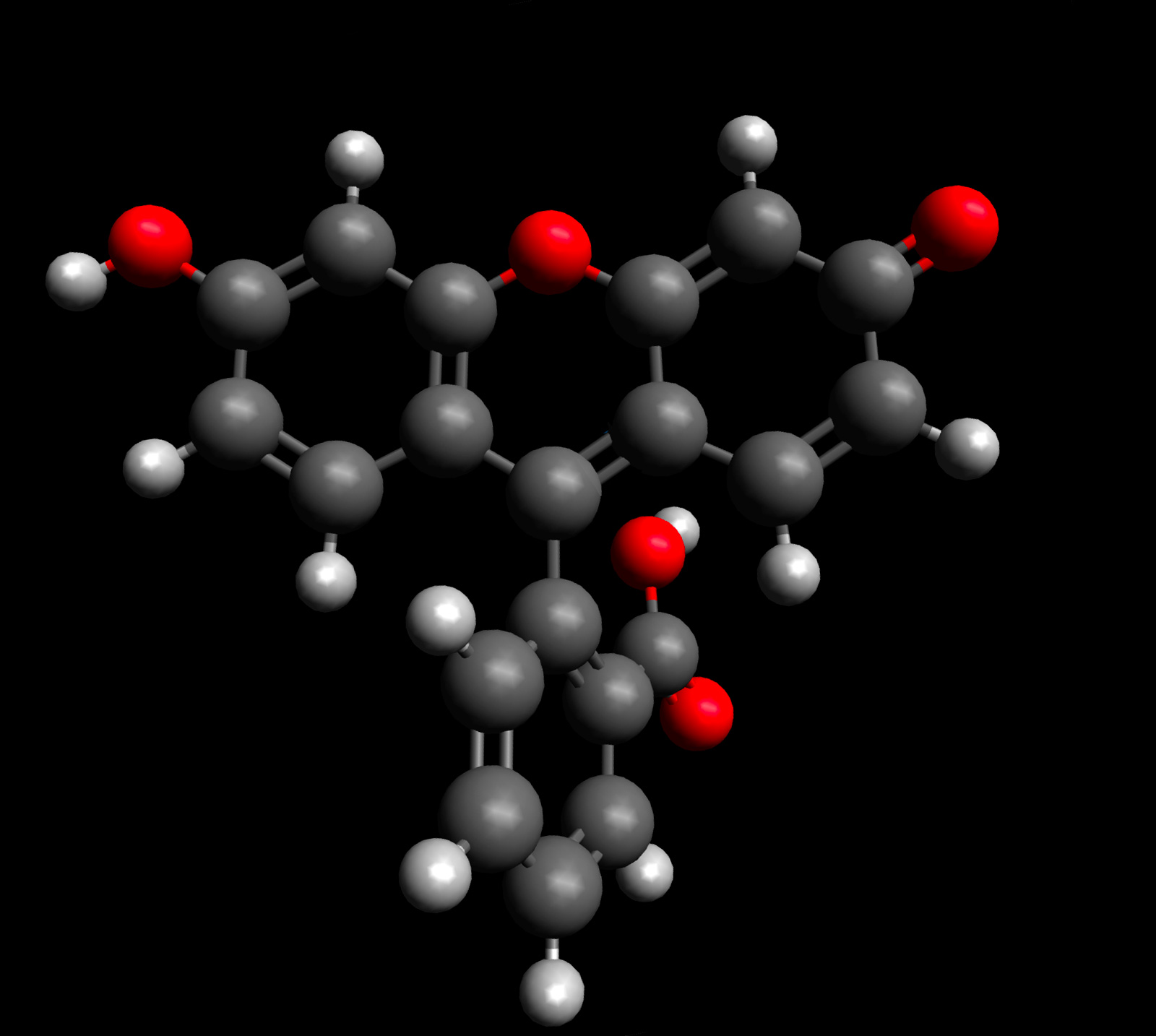
Das Fluorescein-Molekül als Kugel-Stab-Modell
Autor: Ulrich Helmich 2023, Lizenz: Public domain
Auf diesem Bild sieht man die Drehung des Phenylrings sehr gut. Das Molekül-Modell wurde mit der Mac-Version der Software Avogadro erstellt, dann wurde die energetisch günstigste Struktur berechnet.
Herr Prof. Dr. Claus Seidel von der Heinrich-Heine-Universität Düsseldorf hat mich auf die Tatsache mit dem verdrehten Phenylring aufmerksam gemacht, herzlichen Dank dafür nach Düsseldorf! Die Heinrich-Heine-Universität stellt übrigens eine ganze Reihe lehrreicher Videos aus der Reihe "Chemie für Mediziner" zur Verfügung, die wirklich sehr zu empfehlen sind.
Seitenanfang -
Weiter mit Phenolphthalein …