Die homologe Reihe der Alkene
Ethen ist der einfachste Vertreter der homologen Reihe der Alkene. Wie sieht nun der nächst höhere Vertreter aus, das Propen?
Propen
Wir betrachten dazu ein Ethen-Molekül und ersetzen eines der vier H-Atome durch eine Methyl-Gruppe, und schon haben wir das Propen-Molekül:
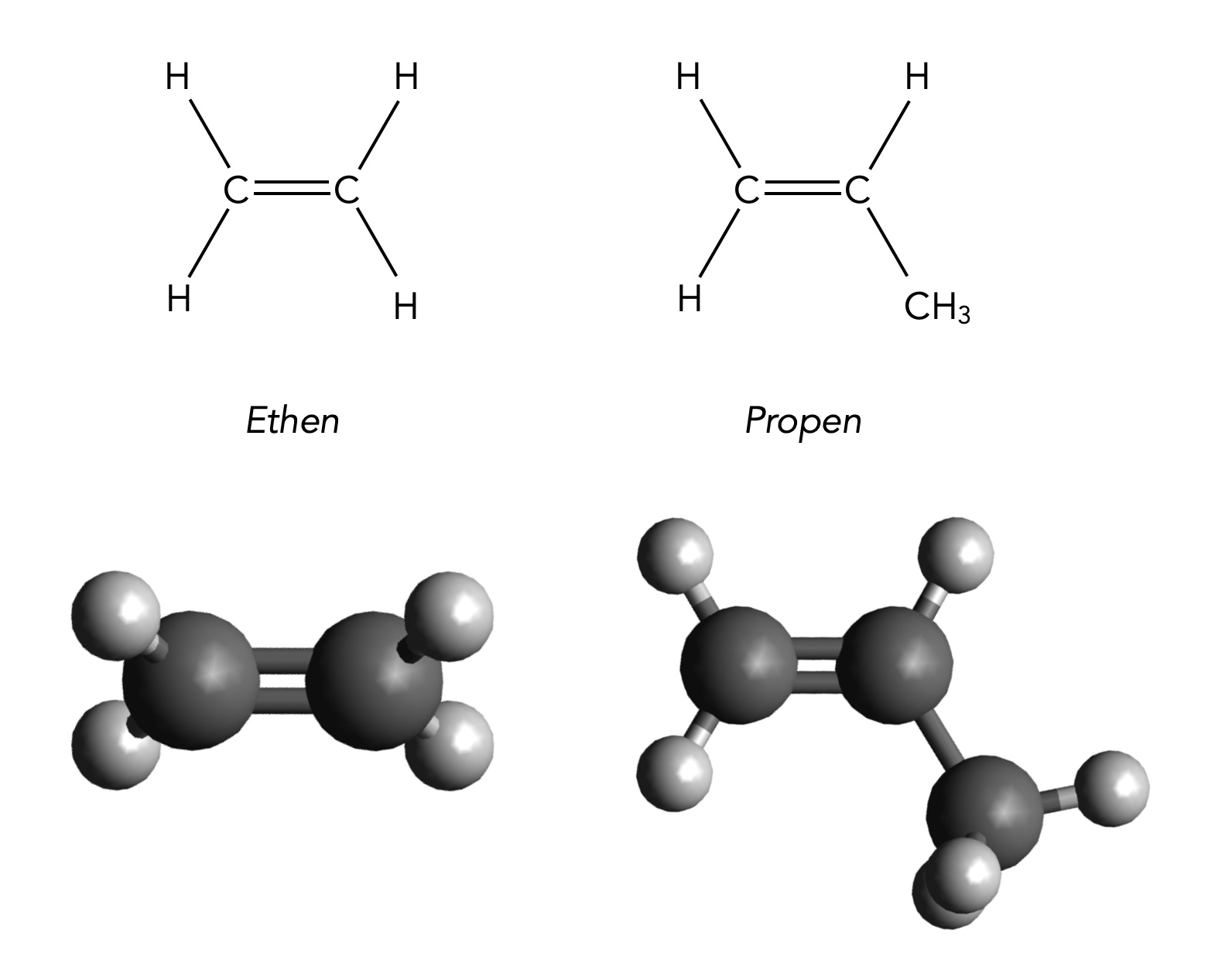
Das Ethen- und das Propen-Molekül im Vergleich
Autor: Ulrich Helmich 11/2024, Lizenz: Public domain
Beim Propen-Molekül liegen die beiden C-Atome der C=C-Doppelbindung, die drei anhängenden H-Atome und das C-Atom der Methyl-Gruppe in einer Ebene. Die Methyl-Gruppe selbst ist dann aber wieder ein räumliches Gebilde, das sich in drei Dimensionen erstreckt.
Keine freie Drehbarkeit
Wenn Sie zwei Kugeln durch zwei feste Stäbe miteinander verbinden, dann können Sie die eine Kugel nicht mehr gegen die andere Kugel verdrehen. Bei einer Verbindung mit nur einem Stab wäre das noch möglich gewesen.
Ähnlich ist es bei den Alkenen mit der C=C-Doppelbindung. Die beiden C-Atome der Doppelbindung können nicht mehr gegeneinander verdreht werden.
Betrachten wir dagegen die C-C-Einfachbindung im Propen-Molekül. Hier kann die CH3-Gruppe um diese Einfachbindung frei gedreht werden.
Buten und die cis-trans-Isomerie
Beim Buten, dem nächsten Vertreter der Alkene, finden wir eine neue Besonderheit. Betrachten Sie dazu die beiden folgenden Molekülmodelle:
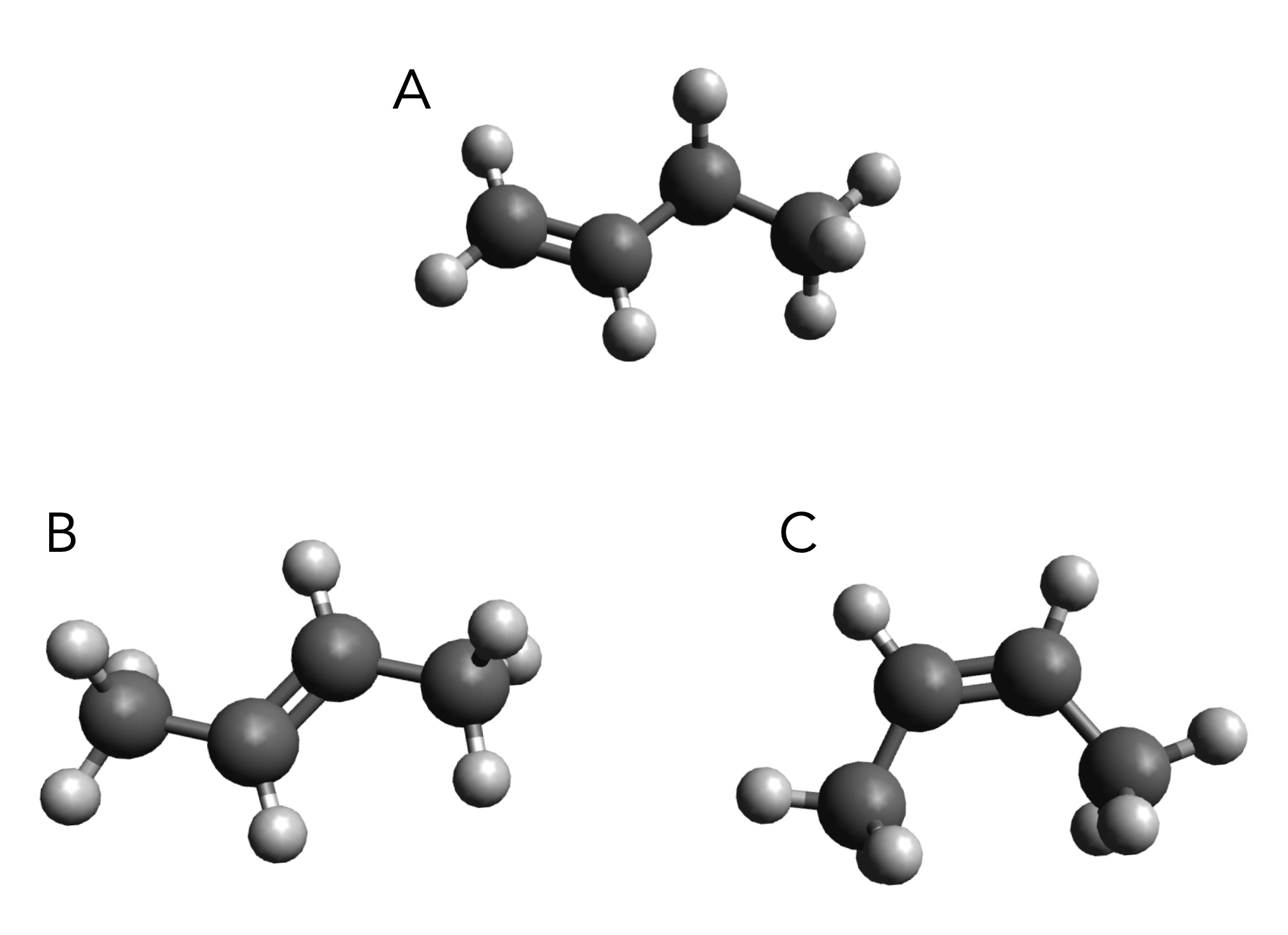
Die drei Butene
Autor: Ulrich Helmich 11/2024, Lizenz: Public domain
Aufgabe 1
Beschreiben Sie die drei abgebildeten Molekülmodelle der drei Buten-Isomere.
Hier geht es zur Lösung dieser Aufgabe.
Was wir hier sehen, ist das erste Beispiel für eine neue Form der Isomerie. Das Isomer B wird als trans-But-2-en bezeichnet, das Isomer C als cis-But-2-en, und das Isomer A ist But-1-en.
Das Präfix "trans" zeigt an, dass sich zwei wichtige Atomgruppen auf entgegengesetzten Seiten der C=C-Doppelbindung aufhalten. Das Präfix "cis" dagegen bedeutet, dass sich die beiden Atomgruppen auf der gleichen Seite der Doppelbindung befinden.
Beim Isomer A macht die Angabe trans oder cis keinen Sinn, weil sich hier nur eine wichtige Atomgruppe an der Doppelbindung befindet, nämlich die Ethyl-Gruppe.
Achten Sie darauf, dass die Präfixe trans und cis stets kursiv geschrieben werden!
Aufgabe 2
Benennen Sie die folgenden Alkene mit ihren korrekten Namen:
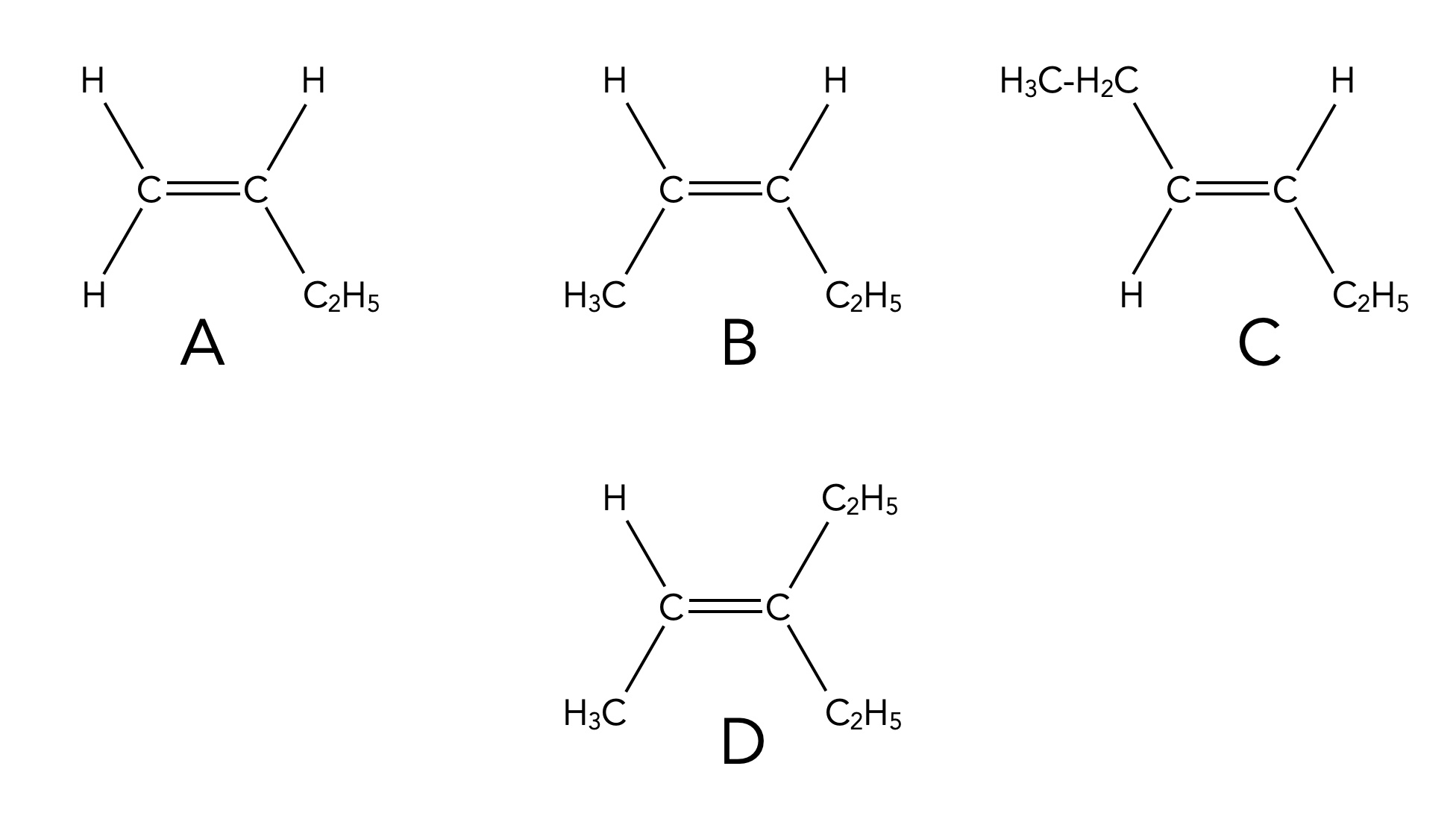
Vier verschiedene Alkene
Autor: Ulrich Helmich 11/2024, Lizenz: Public domain
Der Fall D) ist nur etwas für Experten. Wenden Sie hier Ihre Kenntnisse über die Nomenklatur der Alkane an!
Einen Lösungsvorschlag finden Sie auf dieser Seite.
Hier noch ein paar weitere Beispiele für die Nomenklatur von Alkenen:
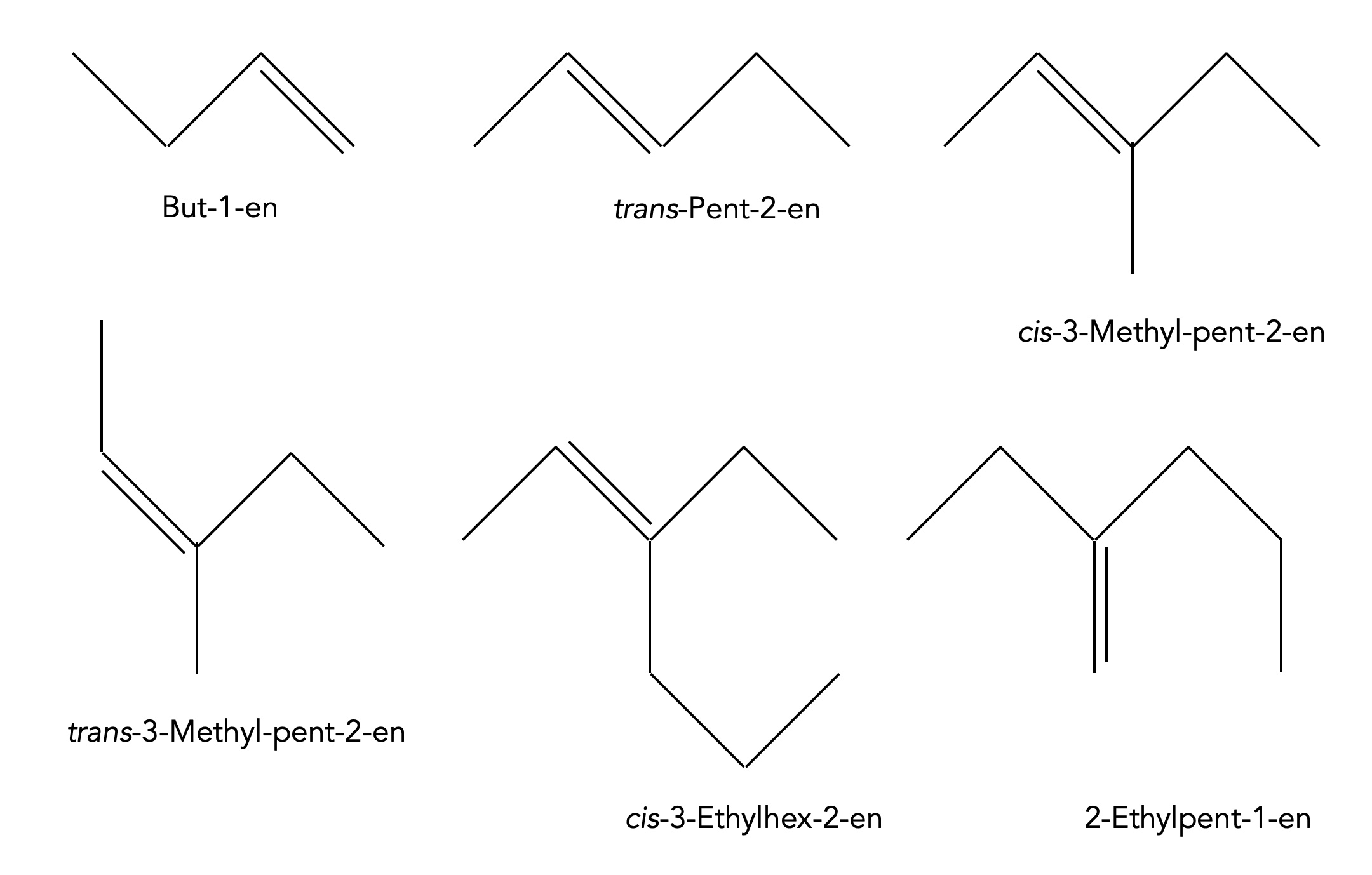
Einige Alkene
Autor: Ulrich Helmich 11/2024, Lizenz: Public domain
Z/E-Nomenklatur
In aktuellen Schulbüchern für die Stufe EF findet sich inzwischen auch die Z/E-Nomenklatur. Alle Alkene, die wir bisher als cis-Alkene bezeichnet haben, können wir nach diesen Regeln auch als Z-Alkene benennen. Das cis-But-2-en kann also auch als Z-But-2-en bezeichnet werden. Der Buchstabe "Z" steht für "zusammen". Alle bisher behandelten trans-Alkene können nach diesen Regeln als E-Alkene bezeichnet werden. Das "E" steht dabei für "entgegengesetzt".
Die Z/E-Nomenklatur ist wesentlich mächtiger als die cis/trans-Nomenklatur, das spielt in der Stufe EF aber noch keine Rolle. Aber Sie sollten zumindest die Begriffe Z und E schon einmal gehört haben und wissen, was sie (ungefähr) bedeuten.
Gut, wenn Sie es unbedingt wissen wollen, müssen Sie auf die Lexikon-Seite zur cis-trans-Isomerie gehen. Ganz unten auf dieser Seite wird die Z/E-Isomerie erläutert.
Physikalische Eigenschaften
Im Prinzip haben alle Kohlenwasserstoff ähnliche physikalische Eigenschaften: Ihre Schmelztemperaturen und Siedetemperaturen sind im Vergleich zu anderen organischen Verbindungen recht niedrig, aber abhängig von der Kettenlänge und der Form der Moleküle. Je länger die Kohlenstoffkette, desto höher diese Temperaturen, und je kompakter die Moleküle, desto niedriger (bis auf einige Ausnahmen).
Auch die Wasserlöslichkeit der Kohlenwasserstoffe ist stets extrem gering, weil die Moleküle keine H-Brücken mit Wasser-Molekülen ausbilden können und daher gezwungenermaßen unter sich bleiben müssen.
Betrachten wir nun zwei verschiedene But-2-en-Isomere:
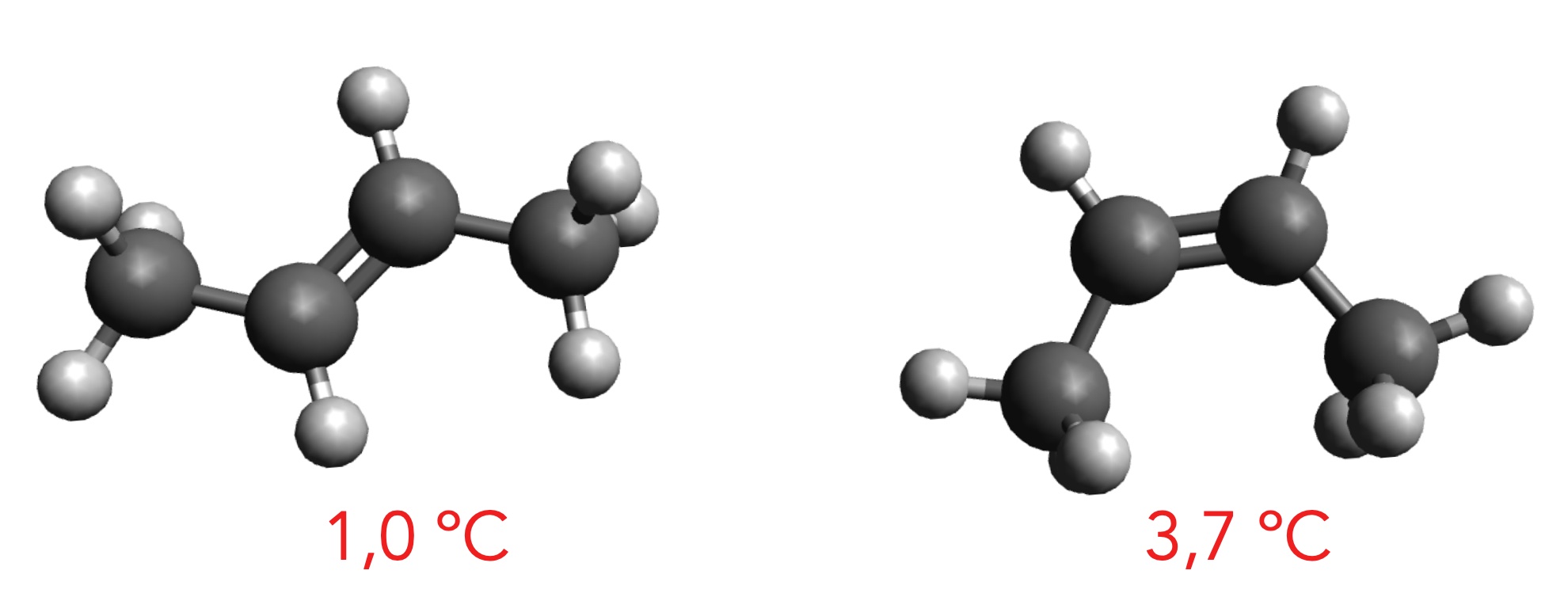
Die Siedetemperaturen von trans- und cis-But-2-en
Autor: Ulrich Helmich 11/2024, Lizenz: Public domain
Aufgabe 3
Finden Sie einen Grund für die unterschiedlichen Siedepunkte der beiden Buten-Isomere.
Eine Lösung mit weiteren Erklärungen finden Sie auf dieser Seite.
Vertiefungsseiten
Auf dieser Seite, für Schüler(innen) der Qualifikationsphase geschrieben, finden Sie weitere Informationen zum Ethen.
Auch im Chemielexikon dieser Homepage finden Sie weiterführende Informationen zum Ethen.
Seitenanfang -
Weiter mit den Reaktionen der Alkene...